Prise en charge de la bilharziose à Schistosoma mansoni dans la zone de santé rurale D’Oicha au Nord Kivu en RD Congo
Management of Schistosoma mansoni bilharzia in the rural health zone of Oicha in North Kivu in the Democratic Republic of Congo.
Bailanda Mumbere Pascal1,2,6, Kimbilwa Katavali Emery7, Kakule Kithanga Jean de Dieu7, Matiaba Binda Paul6, Muyisa Bwambale Quenedy6, Kambale Mbakwiravyo Obede5, Mumbere Muvunga 5, Paluku Kahuka Zephirin7, Kakule Mutsunga Maurice7, Kule Kyusa Archip7, Nzanzu Ndulutulu Joachin 7, Kambale Soheranda Sadraka7, Wembo Ndeo Oscar3, Barhwamire Kabesha Theophile4, Muhindo Sahani Walere2, Paluku Sabuni Louis3.
1.Université Officielle de Semuliki, République Démocratique du Congo
2. Université Catholique du Graben de Butembo, République Démocratique du Congo
3.Université Officielle de Ruwenzori, République Démocratique du Congo
4.Université officielle de Bukavu, République Démocratique du Congo
5.Instittut Supérieur Pédagogique d’Oicha, République Démocratique du Congo
6.Centre Hospitalier le Rocher, République Démocratique du Congo.
7.Zone de santé rurale d’Oicha, République Démocratique du Congo.
Auteur correspondant : drbailanda1@gmail.com,
DOI: https://doi.org/10.53796/hnsj68/9
Identifiant de recherche scientifique arabe: https://arsri.org/10000/68/9
Volume (6) Numéro (8). Pages: 125 - 144
Reçu le: 2025-07-07 | Accepté le: 2025-07-15 | Publié le: 2025-08-01
Résumé: Introduction : La bilharziose est une parasitose chronique d’origine hydrique causée par des trématodes du genre Schistosoma. Le parasite est transmis par contact avec de l’eau douce contaminée contenant des cercaires, formes larvaires issues de mollusques d’eau douce du genre Biomphalaria, hôtes intermédiaires du parasite. Matériel et méthodes : l’étude était menée dans la zone de santé rurale d’Oicha, Territoire de Beni au Nord Kivu en République Démocratique du Congo Il s’agissait d’une étude transversale descriptive qui s’était déroulée durant 3 mois pour une période allant du 1er janvier au 31 Mars 2025, menée sur 316 prestataires soignants confondus. Résultats : 49% âgés de 25 - 34 ans ; 54,7% de sexe féminin ; 75,7% des infirmiers. 65% ;76,7% avec douleurs abdominales ; 68% avec diarrhée ;77% montrent que la schistosomiase se transmet par le contact avec de l’eau contaminée ; 77% administrés le Praziquantel ; 51,25% de rupture de stock des médicaments ; 70,7% ont des toilettes ; 67,7% utilise l’eau de rivière ; 60,3% leurs conditions socio-économiques étaient défavorables ; 86,3% confirme le manque de sensibilisation des communautés ; 68,3% n’avait pas de diagnostic précoce ; 66,3% avait montré que la schistosomiase crée l’incapacité de travailler ; 59,7% montre que leurs enfants avaient abandonnés ; 65,7% de surcharge en raison de la prise en charge de schistosomiase ; 52,7% soutenus par les autorités sanitaires dans la prise en charge. Conclusion : Pour répondre efficacement à l’étude, il est essentiel d’adopter une approche intégrée et durable, combinant le traitement médical, amélioration des conditions d’hygiène et d’assainissement, éducation sanitaire, contrôle des mollusques vecteurs, et implication active de la communauté.
Mots-clés: Prise en charge, bilharziose à Schistosoma mansoni, zone de santé rurale d’Oicha.
Abstract: Introduction: Schistosomiasis is a chronic waterborne parasitic disease caused by trematodes of the genus Schistosoma. The parasite is transmitted by contact with contaminated freshwater containing cercariae, larval forms of freshwater mollusks of the genus Biomphalaria, intermediate hosts of the parasite. Material and methods: The study was conducted in the rural health zone of Oicha, Beni Territory, North Kivu, Democratic Republic of Congo. This was a descriptive, cross-sectional study that took place over a 3-month period from January 1 to March 31, 2025, and included 316 healthcare providers. Results: 49% aged 25-34; 54.7% female; 75.7% nurses. 65%; 76.7% with abdominal pain; 68% with diarrhea; 77% show that schistosomiasis is transmitted through contact with contaminated water; 77% administered Praziquantel; 51.25% drug stockouts; 70.7% have toilets; 67.7% use river water; 60.3% their socioeconomic conditions were unfavorable; 86.3% confirm the lack of community awareness; 68.3% had no early diagnosis; 66.3% had shown that schistosomiasis creates the inability to work; 59.7% show that their children had abandoned them. 65.7% overload due to the management of schistosomiasis; 52.7% supported by health authorities in the management. Conclusion: To effectively address the study, it is essential to adopt an integrated and sustainable approach, combining medical treatment, improvement of hygiene and sanitation conditions, health education, control of snail vectors, and active community involvement.
Keywords: Management, Schistosoma mansoni bilharzia, Oicha rural health zone.
1.Introduction
La bilharziose est une parasitose chronique d’origine hydrique causée par des trématodes du genre Schistosoma. Parmi les différentes espèces, Schistosoma mansoni est responsable de la forme intestinale de la maladie, qui touche principalement les populations vivant dans les régions tropicales et subtropicales, notamment en Afrique subsaharienne, en Amérique du Sud, et au Moyen-Orient [1,2].
Le parasite est transmis par contact avec de l’eau douce contaminée contenant des cercaires, formes larvaires issues de mollusques d’eau douce du genre Biomphalaria, hôtes intermédiaires du parasite. Une fois dans l’organisme humain, les schistosomes se développent, migrent et s’installent dans le système porte, où ils provoquent des dommages significatifs, notamment une fibrose hépatique, une splénomégalie et, dans les cas graves, une hypertension portale [3 ,4].
La bilharziose à S. mansoni constitue un problème majeur de santé publique, surtout dans les zones rurales où l’accès à l’eau potable et à des installations sanitaires est limité. Sa prise en charge nécessite une approche globale qui englobe le diagnostic, le traitement spécifique, la gestion des complications, la prévention communautaire et la surveillance épidémiologique.
Face à la persistance de la transmission malgré les efforts de lutte, il est crucial d’évaluer et d’améliorer les stratégies de prise en charge à travers des programmes intégrés, durables et centrés sur les communautés à risque [5].
Le diagnostic de la bilharziose à Schistosoma mansoni repose sur une combinaison de méthodes parasitologiques, sérologiques, cliniques et parfois d’imagerie. Le choix de la méthode dépend des ressources disponibles, du stade de la maladie et du but (diagnostic individuel, dépistage de masse ou surveillance).
La technique de Kato-Katz permet de détecter les œufs de S. mansoni dans les selles. C’est une méthode simple, peu coûteuse, et quantitative, car elle permet d’estimer la charge parasitaire. Toutefois, sa sensibilité est faible dans les cas de faible infestation ou après traitement.
Autres techniques coprologiques : Concentration par sédimentation ou flottation, moins utilisées en routine mais utiles pour améliorer la détection [6,7,8].
Les tests sérologiques permettent de détecter les anticorps ou les antigènes schistosomiaux dans le sang ou l’urine. La détection d’anticorps (ELISA, IFI, Western blot) : Utile pour identifier les personnes exposées, notamment dans les zones non endémiques ou pour les voyageurs. Cependant, ils ne permettent pas de différencier une infection active d’une ancienne. La détection d’antigènes circulants (CCA, CAA) : ces tests sont plus spécifiques d’une infection active. Le test CCA (Circulating Cathodic Antigen) sur urine est de plus en plus utilisé, car il est rapide et peut être effectué sur le terrain [8, 9,10].
Le PCR (Polymerase Chain Reaction) : très sensible et spécifique, elle permet de détecter l’ADN du parasite dans les selles, le sang ou l’urine. Cette technique est encore peu utilisée dans les pays à faibles ressources en raison de son coût et de la technicité requise.
En Europe, Bien que la bilharziose à Schistosoma mansoni soit historiquement une maladie tropicale, son apparition en Europe, notamment à travers les cas importés ou les foyers autochtones émergents (comme en Corse, France), pose un défi croissant pour les systèmes de santé. Dans un contexte où la maladie est peu connue des professionnels de santé et absente des programmes nationaux de lutte, le diagnostic est souvent tardif, la prise en charge thérapeutique insuffisamment codifiée, et la surveillance épidémiologique lacunaire. Cette situation soulève des enjeux de santé publique, de formation médicale, de migration sanitaire et d’adaptation des politiques de prévention, dans des pays qui ne sont pas historiquement préparés à traiter les maladies parasitaires tropicales [11,12].
En France, Alors que la bilharziose à Schistosoma mansoni est traditionnellement considérée comme une maladie tropicale affectant principalement les régions d’Afrique subsaharienne, son apparition croissante en Europe à travers des cas importés, et plus récemment autochtones (notamment en France), soulève de nouveaux défis sanitaires. Or, les systèmes de santé européens, peu préparés à faire face à cette parasitose, présentent des lacunes en matière de diagnostic précoce, de traitement systématique au praziquantel, et de surveillance épidémiologique. Cette situation met en évidence la nécessité d’adapter les politiques de santé publique, de renforcer la formation médicale sur les maladies tropicales et d’instaurer des protocoles de prise en charge adaptés aux réalités locales et aux risques émergents.
En Asie, S. mansoni est rare comparé à S. japonicum, mais des cas importés par des migrants, des voyageurs ou des travailleurs expatriés peuvent poser un défi de diagnostic.
La faible prévalence entraîne un manque d’attention politique et de ressources allouées à cette forme spécifique de schistosomiase. Les professionnels de santé sont peu formés à reconnaître la bilharziose à S. mansoni, car elle est moins attendue, le diagnostic est souvent tardif ou erroné, car les symptômes intestinaux sont non spécifiques (diarrhée, douleurs abdominales, hépato-splénomégalie) [13].
En Afrique, malgré les efforts déployés depuis plusieurs décennies pour contrôler la bilharziose à Schistosoma mansoni, cette parasitose demeure un important problème de santé publique dans plusieurs pays d’Afrique subsaharienne. La forte prévalence de la maladie est favorisée par des facteurs tels que la pauvreté, l’insuffisance des infrastructures d’assainissement, l’accès limité à l’eau potable, la proximité des populations avec les zones de transmission (rivières, lacs, marigots), et le manque de sensibilisation [14].
De plus, bien que des campagnes de traitement de masse au praziquantel soient mises en œuvre, elles sont souvent irrégulières, mal ciblées ou sous-financées. À cela s’ajoutent la difficulté d’accès aux services de santé dans certaines zones rurales, le manque de personnel formé, l’absence de systèmes efficaces de surveillance-évaluation, et la réinfection rapide des individus traités.
Au Sénégal, la bilharziose intestinale causée par Schistosoma mansoni constitue toujours un problème de santé publique, particulièrement dans les zones rurales et périurbaines situées le long du fleuve Sénégal, dans la vallée et les régions du centre-sud. Malgré les campagnes de traitement préventif de masse au praziquantel initiées dans le cadre des programmes nationaux, la persistance des foyers de transmission, la réinfection rapide des populations traitées et la difficulté d’interrompre le cycle parasitaire posent de sérieux défis [16].
Les facteurs qui compliquent la prise en charge efficace incluent le contact fréquent des populations avec les eaux douces infestées, la faible couverture en eau potable et en infrastructures d’assainissement, l’insuffisance de la surveillance épidémiologique, et le manque de ressources financières et humaines. En outre, l’intégration de la lutte contre la bilharziose dans le système de santé de base reste incomplète, limitant la pérennité des interventions [16].
Au Cameroun, la bilharziose intestinale due à Schistosoma mansoni demeure un problème de santé publique dans plusieurs régions, notamment dans le Littoral, le Nord-Ouest, le Sud-Ouest et certaines zones de l’Adamaoua. Malgré l’existence de programmes de lutte contre les maladies tropicales négligées (MTN), les efforts de prise en charge de la bilharziose sont confrontés à de nombreux obstacles structurels, logistiques et socio-économiques.
La persistance de foyers endémiques s’explique par le contact fréquent des populations avec des plans d’eau infestés, l’insuffisance des infrastructures d’assainissement et d’accès à l’eau potable, ainsi que par une couverture incomplète ou irrégulière des campagnes de traitement de masse au praziquantel. En outre, le système de surveillance épidémiologique reste limité dans plusieurs zones rurales, et les stratégies actuelles manquent d’intégration avec d’autres interventions sanitaires, environnementales et éducatives.
Face à cette situation, comment améliorer la prise en charge globale et durable de la bilharziose à Schistosoma mansoni au Cameroun, en renforçant les capacités locales, en assurant une meilleure coordination intersectorielle, et en adaptant les interventions aux contextes épidémiologiques et socioculturels spécifiques des zones à risque [19]
Le Soudan reste l’un des pays d’Afrique les plus touchés par la bilharziose, en particulier dans sa forme intestinale causée par Schistosoma mansoni. La maladie est endémique dans plusieurs régions, notamment celles traversées par le Nil et ses affluents, où les conditions favorisent la prolifération des mollusques hôtes intermédiaires. Bien que le pays bénéficie du soutien de partenaires internationaux pour la distribution du praziquantel, la prise en charge globale de la maladie demeure insuffisante, fragmentée et peu durable.
Les défis majeurs incluent l’accès limité aux soins de santé, surtout dans les zones rurales et post-conflit, le manque d’eau potable et d’assainissement, la faible couverture des campagnes de traitement de masse, et l’absence de suivi rigoureux après traitement. De plus, les facteurs environnementaux, tels que l’irrigation agricole non contrôlée et les déplacements de populations, augmentent les risques de transmission [20].
Au Kenya, la bilharziose intestinale causée par Schistosoma mansoni représente un défi persistant de santé publique, particulièrement dans les régions proches du lac Victoria, de la vallée du Rift et dans certaines zones côtières. Malgré les efforts du Programme national de lutte contre les maladies tropicales négligées (MTN) et la distribution périodique de praziquantel dans les écoles, la transmission reste active et la maladie continue d’affecter des milliers d’enfants et d’adultes dans les zones endémiques.
La prise en charge de la bilharziose est confrontée à plusieurs difficultés : faible accès à l’eau potable et à l’assainissement, pratiques culturelles favorisant l’exposition aux eaux infestées, couverture incomplète des campagnes de traitement, et manque de suivi post-traitement. De plus, les populations à risque restent souvent mal informées sur les modes de transmission, et les services de santé de première ligne manquent de ressources pour assurer un diagnostic précoce et une prise en charge continue [21].
En Ouganda, la bilharziose intestinale due à Schistosoma mansoni est une maladie endémique majeure, particulièrement prévalente autour du lac Victoria, du lac Albert, ainsi que dans plusieurs districts riverains. Bien que des efforts soutenus aient été entrepris à travers le programme national de lutte contre les maladies tropicales négligées, notamment par la distribution de praziquantel en milieu scolaire, la transmission de la maladie persiste à un niveau préoccupant.
Plusieurs facteurs entravent une prise en charge efficace : le contact fréquent et quotidien des populations avec des eaux infestées, la faible accessibilité à l’eau potable et à des systèmes d’assainissement adéquats, la couverture inégale du traitement de masse, le manque de diagnostic communautaire actif, et l’insuffisance de la sensibilisation des populations sur les risques et les méthodes de prévention. De plus, la réinfection rapide après traitement montre les limites d’une approche centrée uniquement sur la chimiothérapie, sans action simultanée sur les déterminants environnementaux et sociaux [21].
En Tanzanie, la bilharziose intestinale causée par Schistosoma mansoni reste un problème de santé publique majeur, en particulier dans les régions situées le long du lac Victoria, du lac Tanganyika, et dans certaines zones de la vallée du Rift. Malgré la mise en œuvre de programmes nationaux de traitement préventif à base de praziquantel, la prévalence de la maladie demeure élevée dans plusieurs districts, témoignant de la persistance de la transmission. Cette situation s’explique par divers facteurs : l’accès limité à l’eau potable et à des infrastructures d’assainissement, l’exposition quotidienne des populations aux eaux douces infestées, la couverture incomplète et irrégulière des campagnes de traitement, le manque de sensibilisation communautaire, et l’insuffisance des ressources humaines et logistiques dans les services de santé locaux. Par ailleurs, la réinfection rapide après traitement et l’absence d’une stratégie intégrée incluant l’environnement, l’éducation et la surveillance posent un véritable défi [22].
Au Burundi, la bilharziose intestinale due à Schistosoma mansoni constitue une menace persistante pour la santé publique, notamment dans les zones riveraines du lac Tanganyika et dans les vallées humides où les conditions écologiques sont favorables à la transmission. Malgré les interventions du Programme National de Lutte contre les Maladies Tropicales Négligées (MTN), la prévalence de la bilharziose reste préoccupante dans plusieurs localités, affectant surtout les enfants d’âge scolaire et les communautés rurales.
La prise en charge de cette maladie est confrontée à de multiples défis : l’accès limité aux soins de santé dans les zones reculées, l’insuffisance des infrastructures d’assainissement et d’approvisionnement en eau potable, la couverture irrégulière du traitement préventif à base de praziquantel, et la faible sensibilisation des populations aux mesures de prévention
Au Rwanda, la bilharziose intestinale causée par Schistosoma mansoni demeure une maladie parasitaire endémique, particulièrement dans les régions proches des marais, des lacs et des zones humides du pays, notamment dans les districts de l’Est, du Sud et du Nord. Malgré les efforts notables du ministère de la Santé et de ses partenaires à travers le Programme National de Lutte contre les Maladies Tropicales Négligées, les campagnes de traitement préventif à base de praziquantel ne suffisent pas à éliminer la transmission dans les zones les plus exposées.
Les défis majeurs incluent l’accès limité à l’eau potable, l’absence d’infrastructures sanitaires adéquates dans certaines zones rurales, la réinfection rapide après traitement, le manque de sensibilisation des communautés et une surveillance épidémiologique encore incomplète. Par ailleurs, l’intégration insuffisante des actions de lutte contre la bilharziose dans les services de santé primaires, couplée à la nécessité d’impliquer davantage les secteurs de l’éducation, de l’environnement et du développement rural, limite l’efficacité globale des interventions [23].
En République Démocratique du Congo, la bilharziose intestinale due à Schistosoma mansoni reste un important problème de santé publique, particulièrement dans les zones rurales et périurbaines situées le long du fleuve Congo et de ses affluents, ainsi que dans les provinces du Kasaï, de l’Équateur, de la Tshopo et du Tanganyika. Malgré les efforts menés par le Programme National de Lutte contre les Maladies Tropicales Négligées (PNLMTN) en matière de traitement préventif à base de praziquantel, la maladie demeure largement sous-diagnostiquée, sous-traitée et mal surveillée.
Les défis majeurs sont nombreux : insuffisance des données épidémiologiques actualisées, couverture irrégulière des campagnes de traitement de masse, réinfection fréquente des populations traitées, faible accès à l’eau potable et à l’assainissement, éloignement des structures de santé, et manque de sensibilisation des communautés. En outre, l’instabilité de certaines zones, le manque de coordination multisectorielle, et le déficit chronique en ressources humaines et financières compromettent la mise en œuvre efficace et durable des actions de lutte.
À Kinshasa, la bilharziose intestinale à Schistosoma mansoni représente un défi de santé publique, en particulier dans les zones périurbaines et certains quartiers riverains où l’accès à l’eau potable et aux infrastructures d’assainissement est limité. La forte densité de population, associée à des conditions d’hygiène précaires et à une exposition régulière aux eaux stagnantes ou contaminées, favorise la persistance de foyers de transmission.
Malgré les efforts du Programme National de Lutte contre les Maladies Tropicales Négligées et les campagnes ponctuelles de distribution de praziquantel, la couverture reste insuffisante et les interventions sont souvent peu coordonnées. De plus, le diagnostic précoce est rare, et le suivi post-traitement est faible, ce qui entraîne des cas de réinfection fréquents. L’insuffisance de sensibilisation communautaire et le manque d’intégration des actions de lutte dans les structures sanitaires de première ligne compliquent davantage la gestion durable de la maladie.
Au Katanga, région située dans le sud-est de la République Démocratique du Congo, la bilharziose intestinale due à Schistosoma mansoni est un problème de santé publique récurrent, surtout dans les zones rurales et périurbaines proches des cours d’eau et plans d’eau stagnants. Les conditions écologiques favorables, combinées à une faible accessibilité à l’eau potable et à des infrastructures d’assainissement inadéquates, facilitent la transmission continue de la maladie.
La prise en charge de la bilharziose dans cette région fait face à plusieurs difficultés : couverture insuffisante des campagnes de traitement de masse, accès limité aux services de santé, diagnostic tardif, réinfection fréquente, et faiblesse des actions de sensibilisation communautaire. Par ailleurs, les ressources humaines et financières dédiées à la lutte contre la bilharziose restent limitées, et la coordination entre les différents acteurs du secteur santé est souvent insuffisante [24].
Au Bas-Congo (actuel Kongo Central), la bilharziose intestinale causée par Schistosoma mansoni demeure une menace sanitaire importante, notamment dans les zones rurales proches des rivières, lacs et zones humides, où la population est régulièrement en contact avec des eaux contaminées. Malgré les campagnes de traitement par praziquantel menées dans le cadre du Programme National de Lutte contre les Maladies Tropicales Négligées, la transmission persiste, affectant particulièrement les enfants et les communautés vulnérables.
La prise en charge de cette maladie fait face à plusieurs contraintes majeures : faible accès à l’eau potable et aux infrastructures d’assainissement, insuffisance des services de santé de proximité, couverture limitée et irrégulière des traitements de masse, manque de sensibilisation et d’éducation sanitaire, ainsi que la réinfection rapide après traitement. Par ailleurs, les données épidémiologiques actualisées restent rares, limitant la planification efficace des interventions.
En province de l’Équateur, en République Démocratique du Congo, la bilharziose intestinale à Schistosoma mansoni représente un défi sanitaire majeur, particulièrement dans les zones riveraines du fleuve Congo et de ses affluents, ainsi que dans les régions où l’accès à l’eau potable et à l’assainissement est très limité. La forte exposition des populations aux eaux stagnantes infestées, combinée à des conditions socio-économiques défavorables, favorise une transmission continue et une prévalence élevée de la maladie.
La prise en charge de la bilharziose dans cette région est confrontée à plusieurs difficultés : faible couverture des campagnes de traitement de masse, accès limité aux structures de santé, diagnostic tardif et insuffisant, réinfection fréquente, ainsi qu’un déficit en éducation sanitaire et en sensibilisation communautaire. De plus, le manque de données épidémiologiques actualisées entrave la planification et l’optimisation des interventions [24].
Au Maniema, province de la République Démocratique du Congo, la bilharziose intestinale due à Schistosoma mansoni demeure une maladie endémique préoccupante, en particulier dans les zones rurales proches des rivières, des lacs et des zones humides où la population est régulièrement exposée aux eaux infestées. Les conditions socio-économiques difficiles, associées à un accès limité à l’eau potable et à des infrastructures sanitaires insuffisantes, favorisent la persistance de la transmission et un taux élevé d’infection.
La prise en charge de la bilharziose dans cette province est entravée par plusieurs facteurs : une faible couverture des campagnes de traitement de masse à base de praziquantel, l’accès limité aux services de santé, un diagnostic peu systématique, la réinfection rapide après traitement, ainsi qu’une sensibilisation communautaire encore insuffisante. Par ailleurs, le manque de données épidémiologiques actualisées complique la planification et la mise en œuvre efficace des interventions.
En Ituri, province orientale de la République Démocratique du Congo, la bilharziose intestinale à Schistosoma mansoni constitue un problème de santé publique majeur, surtout dans les zones rurales et riveraines où l’exposition aux eaux douces contaminées est fréquente. Les conditions environnementales favorables, combinées à des infrastructures sanitaires précaires, un accès limité à l’eau potable et des conditions socio-économiques difficiles, maintiennent une transmission active et une prévalence élevée de la maladie.
La prise en charge de la bilharziose en Ituri est confrontée à plusieurs défis : couverture insuffisante des campagnes de traitement préventif à base de praziquantel, difficultés d’accès aux services de santé, diagnostic souvent tardif, réinfection rapide, et manque d’éducation sanitaire et de sensibilisation communautaire. De plus, l’instabilité sécuritaire dans certaines zones complique l’organisation et le suivi des interventions [25].
Au Sud-Kivu, province de l’est de la République Démocratique du Congo, la bilharziose intestinale causée par Schistosoma mansoni demeure une maladie endémique, surtout dans les zones rurales et riveraines du lac Tanganyika ainsi que des rivières et marais de la région. Les populations locales, souvent exposées à des eaux contaminées, sont vulnérables à l’infection en raison du manque d’accès à l’eau potable, à des infrastructures sanitaires adéquates et à des services de santé de qualité.
La prise en charge de la bilharziose dans cette province fait face à plusieurs défis majeurs : une couverture insuffisante et irrégulière des campagnes de traitement de masse avec praziquantel, un diagnostic limité et tardif, une réinfection fréquente des patients traités, un manque de sensibilisation communautaire et d’éducation sanitaire, ainsi que des ressources humaines et financières limitées. De plus, l’instabilité sécuritaire et les déplacements de populations compliquent davantage la mise en œuvre efficace des interventions de lutte [25].
Au Nord-Kivu, province de l’est de la République Démocratique du Congo, la bilharziose intestinale à Schistosoma mansoni constitue un problème de santé publique persistant, particulièrement dans les zones rurales et riveraines des lacs, rivières et marais. La population est fortement exposée à la contamination par contact fréquent avec des eaux douces infestées, dans un contexte marqué par un accès limité à l’eau potable, des infrastructures sanitaires insuffisantes, et une pauvreté généralisée.
La prise en charge de la bilharziose dans cette région est freinée par plusieurs défis : couverture inadéquate des campagnes de traitement préventif par praziquantel, difficultés d’accès aux structures sanitaires, diagnostic tardif ou absent, réinfection fréquente, faible sensibilisation communautaire, et manque de ressources humaines et financières. Par ailleurs, l’instabilité sécuritaire et les déplacements de populations aggravent la vulnérabilité des communautés et complexifient la mise en œuvre des programmes de lutte.
Dans le Territoire de Beni, situé au Nord-Kivu en République Démocratique du Congo, la bilharziose intestinale à Schistosoma mansoni demeure une maladie endémique et un problème majeur de santé publique. La forte exposition des populations aux eaux douces contaminées, notamment dans les zones rurales et riveraines des rivières et marais, combinée à un accès limité à l’eau potable et aux infrastructures sanitaires adéquates, favorise la persistance de la transmission .
La prise en charge de la bilharziose dans ce territoire fait face à plusieurs obstacles : faible couverture des campagnes de traitement de masse par praziquantel, accès restreint aux services de santé, diagnostic souvent tardif ou absent, réinfection fréquente, et sensibilisation communautaire insuffisante. En outre, l’instabilité sécuritaire et les déplacements de population liés aux conflits armés compliquent la mise en œuvre efficace des interventions de lutte et limitent l’accès aux soins [25].
En zone de santé d’Oicha, située dans le Territoire de Beni au Nord-Kivu, la bilharziose intestinale à Schistosoma mansoni demeure un problème de santé publique préoccupant. La population est fortement exposée à la contamination par contact fréquent avec les eaux douces stagnantes et contaminées, notamment dans les zones rurales et riveraines, où l’accès à l’eau potable et aux infrastructures sanitaires est limité.
La prise en charge de la bilharziose dans cette zone est entravée par plusieurs facteurs : faible couverture des campagnes de traitement préventif par praziquantel, accès limité aux services de santé, diagnostic insuffisant ou tardif, réinfection rapide, et faible sensibilisation communautaire. Par ailleurs, l’instabilité sécuritaire persistante complique l’organisation et le suivi des interventions sanitaires [26].
Lors de notre étude, nous n’avions pas trouvé la publication scientifique spécifique concernant la prise en charge de la bilharziose à Schistosoma mansoni dans la zone de santé d’Oicha, située dans le territoire de Beni, province du Nord-Kivu, en République Démocratique du Congo (RDC). Les études disponibles se concentrent principalement sur d’autres provinces, telles que l’Ituri et le Kongo Central.
Cependant, des recherches similaires menées dans des provinces voisines, comme l’Ituri, offrent des informations pertinentes sur la situation épidémiologique de la schistosomiase dans la région. Par exemple, une étude menée en 2017 dans la province de l’Ituri a révélé une prévalence élevée de l’infection à Schistosoma mansoni, atteignant jusqu’à 95 % dans certaines zones. Les facteurs de risque identifiés comprenaient l’exposition aux eaux locales, le manque d’assainissement et l’absence de latrines familiales. Ces résultats suggèrent que la situation épidémiologique dans la zone de santé d’Oicha pourrait être similaire, compte tenu de la proximité géographique et des conditions environnementales comparables [26].
Pour obtenir des informations spécifiques sur la situation de la schistosomiase dans la zone de santé d’Oicha, il serait pertinent de consulter les autorités sanitaires locales ou les programmes de lutte contre les maladies tropicales négligées (MTN) opérant dans la région.
Dans ce contexte, comment mettre en place une stratégie efficace, durable et adaptée aux réalités locales pour la prise en charge intégrée de la bilharziose à Schistosoma mansoni en zone de santé rurale d’Oicha, combinant le traitement, la prévention, l’amélioration des conditions d’hygiène et disponibiliser l’eau potable à la population et le renforcement du système de santé et mobilisation communautaire, tout en tenant compte des contraintes sécuritaires ?
Objectif général
Décrire la prise en charge de la bilharziose à Schistosoma mansoni dans la zone de santé d’Oicha, en améliorant l’accès au diagnostic, au traitement efficace, à la prévention et à la sensibilisation communautaire, tout en renforçant les capacités du système de santé local.
Objectifs spécifiques
1.Assurer une couverture optimale des campagnes de traitement de masse par praziquantel auprès des populations à risque dans la zone de santé d’Oicha.
2.Améliorer l’accès à l’eau potable et aux infrastructures d’assainissement pour réduire le contact avec les eaux contaminées.
3.Mettre en place un système de surveillance épidémiologique efficace pour le suivi et l’évaluation des interventions contre la bilharziose.
4.Promouvoir la collaboration intersectorielle entre les secteurs de la santé, de l’environnement, de l’éducation et de l’eau pour une lutte intégrée.
2.Matériel et méthodes
2.1. Cadre de l’étude
Notre étude est menée dans la zone de santé rurale d’Oicha se situant dans le Territoire de Beni au Nord Kivu en République Démocratique du Congo, couvre une superficie de 1.656 Km2, située latitude Est 77696,989 m, longitude Nord 780671,652 m, altitude 1050,9 m avec une précision de 1,5 m et une population de 341.730 habitants répartis dans 27 aires de santé.
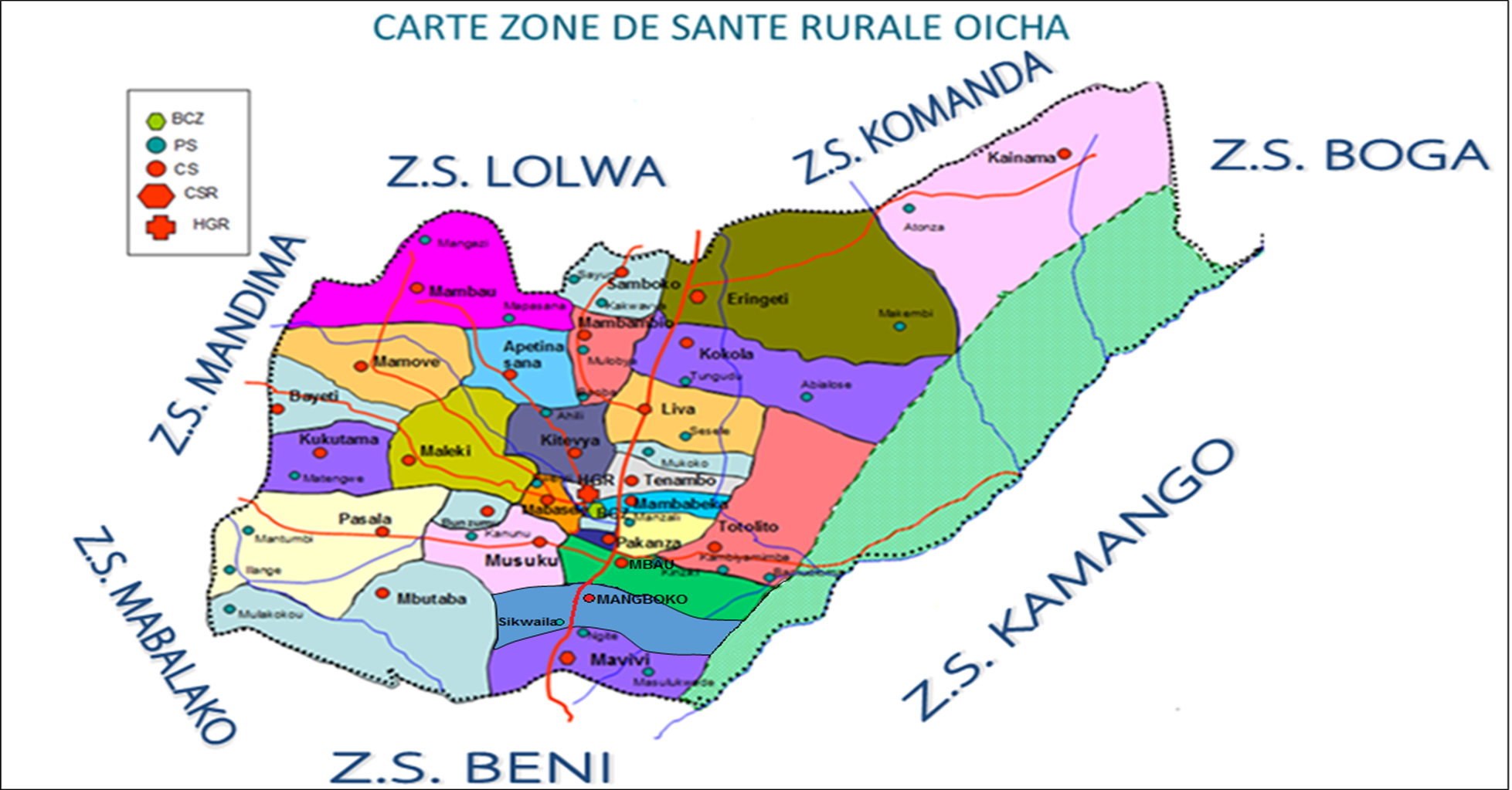
Figure 1. Carte postale de la zone de santé rurale d’Oicha
2.2.Type d’étude, période et cible de l’étude
Il s’agit d’une étude transversale descriptive qui s’est déroulée durant 3 mois pour une période allant du 1er janvier au 31 Mars 2025. La population cible de l’étude est constituée de tous les personnels soignants confondus (médecins, infirmiers, laborantins et pharmacienne) œuvrant et enregistrés dans la zone de santé.
2.3. Variables de l’étude
Les variables indépendantes : les facteurs socio-professionnels, le niveau de connaissance, la pratique de la prise en charge, les obstacles, disponibilité des intrants, la perception, la sensibilisation communautaire et l’impact de la prise en charge.
La variable dépendante : Bilharziose à Schistosoma mansoni
2.4. Taille et population d’étude
La taille de l’échantillon était donnée par le bureau central de la zone de santé rurale d’Oicha, soit un effectif de 316 personnels soignants.
2.6. Critères d’éligibilité
Critères d’inclusion : tous personnels soignants de la zone de santé rurale d’Oicha, être reconnu par la zone de santé, travailler dans une des structures des soins de la zone de santé, être disponible et accepter de participer à l’étude.
Critères de non inclusion : tous critères contraires aux critères d’inclusion.
2.7. Techniques de collecte des données
La revue documentaire a permis de consulter différents ouvrages, articles et rapports de la zone de santé rurale d’Oicha, afin d’aborder l’état de la question et la problématique de l’étude ainsi que des données ayant appuyé les discussions des résultats trouvés.
Pour réaliser l’étude, nous avons d’abord utilisé l’interview couplée au questionnaire lié à la prise en charge. Le questionnaire est soumis aux personnels soignants qui savent lire et écrire pour recueillir leurs opinions par rapport à la thématique de recherche, il contient les questions ouvertes et sont expliquées en langue locale pour une meilleure compréhension ; les réponses fournies sont prises en compte et enregistrées directement sur le questionnaire.
2.8. Collecte, analyse et traitement des données
Nous avons distribué les questionnaires à nos enquêtés, après explication. La récolte des données était faite dans le respect strict des critères d’éligibilité et le raffinage du questionnaire qui a été plus protesté a permis de réduire le risque de biais.
L’enregistrement des données collectées était fait sur le questionnaire, le logiciel Microsoft Word 2010, Excel 2010 tandis que l’analyse des données était faite à l’aide de SPSS 27.
2.9. Considérations éthiques
L’étude avait obtenu une autorisation du comité d’éthique médicale de l’Université de Goma, en République Démocratique du Congo par l’attestation N° Approbation : UNIGOM/CEM/010/2023 du 01 Mars 2023.
Nous avions contacté les autorités politico administratives locales pour visa et autorisation de l’étude dans la zone de santé rurale d’Oicha.
Le consentement libre et éclairé des enquêtés était obtenu oralement après les explications en rapport avec l’étude à mener dans la zone de santé. L’enquêté était informé qu’il était libre de refuser ou de se retirer lors de l’étude et aucune sanction était prévue.
Pour garder l’intégrité, la discrétion, la confidentialité nous avions procédé à l’anonymat des enquêtés et des données recueillies spécialement pour la recherche.
Résultats
Tableau 1. Facteurs socio démographiques
|
Age de l’enquêté |
Fréquence |
% |
|
Moins de 25 ans |
55 |
18,3 |
|
[25 – 34 ans] |
147 |
49 |
|
[35 – 44 ans] |
67 |
22,3 |
|
[45 et plus] |
31 |
10,3 |
|
Sexe de l’enquêté |
||
|
Masculin |
136 |
45,3 |
|
Féminin |
164 |
54,7 |
|
Poste actuel de l’enquêté |
||
|
Médecin |
25 |
8,3 |
|
Infirmier |
227 |
75,7 |
|
Pharmacien |
48 |
16 |
|
Ancienneté dans le métier |
||
|
Moins de 2 ans |
111 |
37 |
|
2-5 ans |
116 |
38,7 |
|
6-10 ans |
51 |
17 |
|
Plus, de 10 ans |
22 |
7,3 |
De ce tableau 1, nous constatons que 49% des répondants avait l’âge variant entre 25 – 34 ans ; 54,7% des répondants était du sexe féminin ; 75,7% était des infirmier(res) ; 38,7% à une ancienneté de 2 à 5 ans.
Tableau 2. Les Facteurs sanitaires
|
Avoir déjà fait une formation spécifique sur la schistosomiase |
Fréquence |
Pourcentage |
|
Oui |
213 |
71 |
|
Non |
87 |
29 |
|
Sang dans les urines |
||
|
Oui |
105 |
35 |
|
Non |
195 |
65 |
|
Douleurs abdominales |
||
|
Oui |
230 |
76,7 |
|
Non |
70 |
23,3 |
|
Fatigue chronique |
||
|
Oui |
60 |
20 |
|
Non |
240 |
80 |
|
Diarrhée |
||
|
Oui |
96 |
32 |
|
Non |
204 |
68 |
|
Retard de croissance chez les enfants |
||
|
Oui |
39 |
13 |
|
Non |
261 |
87 |
Il ressort de ce tableau 2 que 71% des répondants avait déjà participé à une formation spécifique sur la schistosomiase ; 65% n’avait pas le sang dans les urines ; 76,7% avait des douleurs abdominales ; 80% n’avait pas des fatigues chroniques ; 68% n’avait pas des symptômes de la diarrhée ; 87% n’avait pas de retard de croissance chez les enfants.
Tableau 3. Diagnostique des cas de schistosomiase
|
Diagnostique régulièrement des cas de schistosomiase |
Fréquence |
Pourcentage |
|
Oui |
195 |
65 |
|
Non |
105 |
35 |
|
Total |
300 |
100 |
De ce tableau 3, nous constatons que 65% des répondants sont diagnostiqué régulièrement des cas de la schistosomiase contre 35%.
Tableau 4. Information sur la Voie de transmission de la schistosomiase
|
Voie de transmission de la schistosomiase |
Fréquence |
Pourcentage |
|
Par contact avec de l’eau contaminée |
231 |
77,0 |
|
Par consommation d’eau non potable |
56 |
18,7 |
|
Par les moustiques |
6 |
2,0 |
|
Je ne sais pas |
7 |
2,3 |
|
Total |
300 |
100,0 |
De ce tableau 4, nous constatons que 77% des répondants avait montré que la schistosomiase se transmet par le contact avec de l’eau contaminée et 18% montre que c’est par la consommation d’eau non potable.
Tableau 5. Informations sur outils de diagnostique de la schistosomiase
|
Analyse clinique |
Fréquence |
Pourcentage |
|
Oui |
109 |
36,3 |
|
Non |
191 |
63,7 |
|
Analyse des selles |
||
|
Oui |
231 |
77 |
|
Non |
69 |
23 |
|
Signes cliniques |
||
|
Oui |
48 |
16 |
|
Non |
252 |
84 |
Il ressort de ce tableau 5 que 63,7% des répondants n’avait pas fait une analyse d’urine ; 77% avait fait l’analyse de selles.
Tableau 6. Informations sur le traitement de la schistosomiase
|
Traitement principal administré par l’enquêté |
Fréquence |
Pourcentage |
|
Praziquantel |
231 |
77 |
|
Remèdes traditionnels (en collaboration avec les patients) |
32 |
10,7 |
|
Vaccination |
37 |
12,3 |
|
Avoir déjà rencontré des difficultés pour administrer un traitement |
||
|
Oui |
160 |
53,3 |
|
Non |
140 |
46,7 |
|
Ruptures de stock de médicaments |
||
|
Oui |
82 |
51,25 |
|
Non |
78 |
48,75 |
|
Coût élevé du traitement pour les patients |
||
|
Oui |
86 |
53,8 |
|
Non |
74 |
46,3 |
|
Refus de traitement par les patients |
||
|
Oui |
71 |
44,4 |
|
Non |
89 |
55,6 |
De ce tableau 6, nous constatons que 77% leur traitement les administrés était le Praziquantel ; 53,3% avait eu des difficultés pour administrer un traitement ; 51,25% avait montré que la difficulté était la rupture de stock des médicaments ; 53,8% certifie que c’était le cout élevé du traitement ; 55,6% des patients ne refusait pas le traitement.
Tableau 7. Les Facteurs de risque de la schistosomiase
|
Facteurs |
Fréquence |
Pourcentage |
|
Absence de latrines |
||
|
Oui |
88 |
29,3 |
|
Non |
212 |
70,7 |
|
Utilisation d’eau de rivières ou de sources |
||
|
Oui |
203 |
67,7 |
|
Non |
97 |
32,3 |
|
Conditions socio-économiques défavorables |
||
|
Oui |
181 |
60,3 |
|
Non |
119 |
39,7 |
|
Manque de sensibilisation des communautés |
||
|
Oui |
259 |
86,3 |
|
Non |
41 |
13,7 |
|
Absence de diagnostic précoce |
||
|
Oui |
95 |
31,7 |
|
Non |
205 |
68,3 |
|
Insuffisance de médicaments disponibles |
||
|
Oui |
79 |
26,3 |
|
Non |
221 |
73,7 |
|
Infrastructure sanitaire inadequate |
||
|
Oui |
42 |
14 |
|
Non |
258 |
86 |
|
Avis sur la suffisance de la formation du personnel sur la schistosomiase |
||
|
Oui |
186 |
62 |
|
Non |
114 |
38 |
|
Formation continue pour le personnel de santé |
||
|
Oui |
194 |
64,7 |
|
Non |
106 |
35,3 |
|
Fourniture régulière en intrants |
||
|
Oui |
85 |
28,3 |
|
Non |
215 |
71,7 |
Il ressort de ce tableau 7 que 70,7% des répondants avait confirmé avoir des toilettes ; 67,7% utilise l’eau d rivière ou de source ; 60,3% leurs conditions socio-économiques étaient défavorables ; 86,3% confirme le manque de sensibilisation des communautés ; 68,3% n’avait pas de diagnostic précoce ; 73,7% n’avait pas confirmé l’insuffisance de médicaments disponibles ; 86% montre que les infrastructures sanitaires sont adéquates ; 62% confirme la suffisance du personnel sur la schistosomiases ; 64,7% avait confirmé une formation continue pour le personnel de santé ; 71,7% n’avait pas des fournitures régulière en intrants.
Tableau 8. Les Facteurs de risque de la schistosomiase (suite)
|
Amélioration des infrastructures sanitaires |
Fréquence |
Pourcentage |
|
Oui |
88 |
29,3 |
|
Non |
212 |
70,7 |
|
Campagne de sensibilisation Communautaire |
||
|
Oui |
157 |
52,3 |
|
Non |
143 |
47,7 |
|
Avis de l’enquêté sur le fait que la schistosomiase soit un problème de santé publique important |
||
|
Oui |
231 |
77 |
|
Non |
45 |
15 |
|
Je ne sais pas |
24 |
8 |
|
A déjà participé aux campagnes de sensibilisation |
||
|
Oui |
166 |
55,3 |
|
Non |
134 |
44,7 |
|
A une position favorable sur renforcement de collaboration avec les leaders communautaires |
||
|
Oui |
236 |
78,7 |
|
Non |
53 |
17,7 |
|
Je ne sais pas |
11 |
3,7 |
De ce tableau 8 70,7% confirme qu’il n’existe pas l’amélioration des infrastructures sanitaires ; 52,3% confirme qu’il y a des campagnes de sensibilisation communautaire ; 77% avait montré que la schistosomiase est un problème de santé publique important ; 55,3% avait déjà participé aux campagnes de sensibilisation ; 78,7% confirme une position favorable sur renforcement de collaboration avec les leaders communautaires.
Tableau 9. Impact de schistosomiase
|
Incapacité à travailler |
Fréquence |
Pourcentage |
|
Oui |
199 |
66,3 |
|
Non |
101 |
33,7 |
|
Abandon scolaire des enfants |
||
|
Oui |
121 |
40,3 |
|
Non |
179 |
59,7 |
|
Dépenses élevées pour les ménages |
||
|
Oui |
164 |
54,7 |
|
Non |
136 |
45,3 |
|
Marginalisation sociale |
||
|
Oui |
65 |
21,7 |
|
Non |
235 |
78,3 |
Il ressort de ce tableau 9 que 66,3% avait montré que la schistosomiase crée l’incapacité de travailler ; 59,7% montre que leurs enfants avaient abandonnés l’école ; 54,7% avait montré que les dépenses du ménage sont élevées ; 78,3% n’impacte pas la marginalisation sociale.
Tableau 10. Prise en charge de la schistosomiase
|
Variables |
Fréquence |
Pourcentage |
|
Ressent une surcharge en raison de la prise en charge de schistosomiase |
||
|
Oui |
197 |
65,7 |
|
Non |
103 |
34,3 |
|
Estime être suffisamment soutenu par les autorités sanitaires dans la prise en charge |
||
|
Oui |
158 |
52,7 |
|
Non |
142 |
47,3 |
De ce tableau 10, nous constatons que 65,7% confirme le fait de ressentir une surcharge en raison de la prise en charge de schistosomiase ; 52,7% estime être suffisamment soutenu par les autorités sanitaires dans la prise en charge.
Discussion
Les résultats confirment une prise en charge de la bilharziose à Schistosoma mansoni dans la zone se santé rurale d’Oicha. Les facteurs sociodémographiques, les Facteurs sanitaires, les facteurs sanitaires, les facteurs de risques et les informations sur la maladie jouent un grand rôle dans la prise en charge. Un renforcement des mesures de lutte intégrée s’avère nécessaire : traitement antiparasitaire en masse, amélioration de l’accès à l’eau potable, assainissement, et éducation communautaire.
Facteurs socio démographiques
Du tableau 1, nous constatons que 49% des répondants avait l’âge variant entre 25 – 34 ans ; 54,7% des répondants était du sexe féminin ; 75,7% était des infirmier(res) ; 38,7% à une ancienneté de 2 à 5 ans. La prise en charge de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha peut être efficace avec une compréhension fine du contexte sociodémographique local. Ces facteurs conditionnent à la fois la dynamique de transmission, l’accès aux soins et l’efficacité des interventions de santé publique.
Une prise en charge efficace de la bilharziose à Schistosoma mansoni devra être adaptée aux réalités sociodémographiques dans la zone de santé. Ce résultat corrobore avec ceux trouvés par [1,2, 3] se rapportant à une approche communautaire sensible au genre, à l’âge, à la pauvreté et à l’éducation est indispensable pour obtenir une réduction durable de la transmission et améliorer l’accès équitable aux soins.
Mais aussi la bilharziose touche principalement les enfants d’âge scolaire (5 à 14 ans), car ils passent plus de temps à jouer ou à se baigner dans les eaux contaminées. Les hommes adultes, notamment les pêcheurs, cultivateurs et laveurs de sable, sont également exposés. Les femmes sont souvent contaminées lors des activités ménagères comme la lessive ou la vaisselle dans les rivières. Cette distribution par âge et par sexe implique que les campagnes de traitement doivent cibler des groupes spécifiques, et pas uniquement les enfants, ce résultat est similaire à celui trouvé par [5,6].
Les Facteurs sanitaires
Il ressort du tableau 2 que 71% des répondants avait déjà participé à une formation spécifique sur la schistosomiase ; 65% n’avait pas le sang dans les urines ; 76,7% avait des douleurs abdominales ; 80% n’avait pas des fatigues chroniques ; 68% n’avait pas des symptômes de la diarrhée ; 87% n’avait pas de retard de croissance chez les enfants. La lutte contre la bilharziose dans les zones de santé endémiques repose sur un ensemble d’interventions sanitaires, incluant le diagnostic, le traitement, la prévention et la surveillance épidémiologique. Toutefois, plusieurs contraintes limitent l’efficacité de la réponse sanitaire à cette maladie parasitaire. Ce résultat coïncide avec ceux trouvés par [7,8,9] qui stipulent que dans la majorité des zones de santé concernées, le système de santé primaire est sous-équipé, avec un manque de personnel formé, de laboratoires fonctionnels et de médicaments essentiels. Cela réduit la capacité des structures sanitaires à détecter, traiter et suivre les cas de bilharziose de manière efficace. Le personnel de santé, parfois non sensibilisé à la schistosomiase, peut négliger les symptômes légers ou les confondre avec d’autres pathologies gastro-intestinales. Le médicament de référence, le Praziquantel, est en principe fourni gratuitement dans le cadre des campagnes de traitement de masse (PTME) soutenues par l’OMS et le ministère de la Santé. Toutefois, des ruptures de stock sont fréquentes, particulièrement entre deux campagnes. Hors campagne, l’accès au Praziquantel dans les structures sanitaires reste limité, voire inexistant pour les patients qui consultent de manière individuelle [10, 11,12]. L’insuffisance d’activités de sensibilisation communautaire et l’absence de matériel éducatif dans les langues locales limitent la prévention. La prévention repose sur l’amélioration de l’accès à l’eau potable, la construction de latrines et la réduction des contacts avec les eaux contaminées, ce qui nécessite des approches intersectorielles (santé, éducation, WASH).
Diagnostique des cas de schistosomiase et informations sur outils de diagnostique de la schistosomiase
Des tableaux 3 et 4, nous constatons que 77% des répondants avait montré que la schistosomiase se transmet par le contact avec de l’eau contaminée et 18% montre que c’est par la consommation d’eau non potable, 77% des répondants avait montré que la schistosomiase se transmet par le contact avec de l’eau contaminée et 18% montre que c’est par la consommation d’eau non potable. Le diagnostic des cas de schistosomiase constitue une étape cruciale dans la chaîne de prise en charge, car il conditionne l’identification des malades, l’administration du traitement, ainsi que la surveillance de l’efficacité des programmes de lutte. Dans les zones de santé endémiques, plusieurs défis limitent une détection optimale des cas. Les méthodes de diagnostic disponibles : Méthode de Kato-Katz (examen parasitologique des selles), C’est la méthode standard recommandée par l’OMS pour le diagnostic des cas de bilharziose intestinale, le test CCA (Circulating Cathodic Antigen) : Test rapide réalisé sur l’urine, détectant les antigènes circulants produits par le parasite. De plus, le diagnostic clinique (basé sur les symptômes comme les douleurs abdominales, diarrhée sanglante ou hépatosplénomégalie) est non spécifique, conduisant parfois à des sous-diagnostics ou à des traitements inappropriés ; ces résultats sont semblables à ceux trouvés par [13,14,16]
Information sur la voie de transmission de la schistosomiase
La bilharziose à Schistosoma mansoni suit un cycle biologique complexe impliquant un hôte intermédiaire (les mollusques du genre Biomphalaria) et un hôte définitif (l’être humain). Le cycle comprend les étapes suivantes : Les œufs de S. mansoni sont excrétés dans les selles humaines et atteignent les plans d’eau douce ; Ils éclosent en miracidiums, qui infectent les mollusques ; Après multiplication dans le mollusque, ils libèrent des cercaires, formes infestantes qui nagent librement dans l’eau ; Les cercaires pénètrent la peau humaine au contact de l’eau contaminée selon [18,19].
Informations sur le traitement de la schistosomiase
En partant du tableau 6, nous constatons que 77% leur traitement les administrés était le Praziquantel ; 53,3% n’avait pas eu des difficultés pour administrer un traitement ; 51,25% avait montré que la difficulté était la rupture de stock des médicaments ; 53,8% certifie que c’était le cout élevé du traitement ; 55,6% des patients ne refusait pas le traitement. Le traitement de la schistosomiase est un pilier fondamental de la stratégie de lutte contre cette parasitose. Dans la zone de santé endémique, le traitement vise non seulement à soigner les cas individuels, mais aussi à réduire la transmission communautaire. Toutefois, plusieurs facteurs influencent l’efficacité et l’équité de ce traitement dans le contexte local [26]. Le traitement de la schistosomiase à S. mansoni repose principalement sur le Praziquantel, administré dans le cadre de campagnes de masse ou à titre individuel. Une prise en charge efficace nécessite de garantir la disponibilité continue du médicament, d’améliorer la couverture et l’acceptabilité, et de renforcer le système de suivi thérapeutique. Le succès à long terme repose également sur la prévention de la ré infestation par l’amélioration des conditions d’eau et d’hygiène selon [25, 26].
Les Facteurs de risque de la schistosomiase
Il ressort de ce tableau 7 et 8 que 70,7% des répondants avait confirmé avoir des toilettes ; 67,7% utilise l’eau d rivière ou de source ; 60,3% leurs conditions socio-économiques étaient défavorables ; 86,3% confirme le manque de sensibilisation des communautés ; 68,3% n’avait pas de diagnostic précoce ; 73,7% n’avait pas confirmé l’insuffisance de médicaments disponibles ; 86% montre que les infrastructures sanitaires sont adéquates ; 62% confirme la suffisance du personnel sur la schistosomiases ; 64,7% avait confirmé une formation continue pour le personnel de santé ; 71,7% n’avait pas des fournitures régulière en intrants. La compréhension des facteurs de risque liés à la schistosomiase est indispensable pour une prise en charge efficace et ciblée. Selon [20,21], ces facteurs influencent la dynamique de transmission de Schistosoma mansoni et permettent d’identifier les groupes et zones prioritaires dans une stratégie de lutte intégrée. Dans une zone de santé endémique, les facteurs de risque de la schistosomiase sont multiples et interconnectés : environnementaux, comportementaux, économiques, démographiques et structurels. La prise en charge efficace doit donc adopter une approche multidimensionnelle, combinant traitement médical, éducation sanitaire, amélioration des infrastructures, et lutte contre les mollusques vecteurs.
Impact de la bilharziose à Schistosoma mansoni
Il ressort de ce tableau 9 que 66,3% avait montré que la schistosomiase crée l’incapacité de travailler ; 59,7% montre que leurs enfants avaient abandonnés l’école ; 54,7% avait montré que les dépenses du ménage sont élevées ; 78,3% n’impacte pas la marginalisation sociale. Selon [21,22,23], la bilharziose à Schistosoma mansoni, a un impact multidimensionnel dans les zones de santé où elle est endémique. En plus des effets directs sur la santé humaine, elle a des répercussions économiques, éducatives et sociales, ce qui complique sa prise en charge globale. La schistosomiase à Schistosoma mansoni a un impact profond et durable sur les individus, les familles et l’ensemble du système de santé d’une zone endémique. Réduire cet impact nécessite une approche intégrée, préventive et curative, mais aussi sociale, en associant les communautés locales, les écoles et les autorités sanitaires à tous les niveaux de la réponse.
Prise en charge de la schistosomiase
De ce tableau 10, nous constatons que 65,7% confirme le fait de ressentir une surcharge en raison de la prise en charge de schistosomiase ; 52,7% estime être suffisamment soutenu par les autorités sanitaires dans la prise en charge. La prise en charge de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha repose sur une approche intégrée, combinant le traitement curatif, la prévention, la surveillance épidémiologique et la mobilisation communautaire. Les résultats de [23 ,24,25] prouvent que la prise en charge doit tenir compte des spécificités locales (environnementales, sociales, économiques) pour être efficace. Elle ne doit pas se limiter au traitement médicamenteux. Elle exige une approche globale incluant le dépistage précoce, la réduction des risques environnementaux, la mobilisation communautaire, ainsi que la coordination multisectorielle. C’est à ce prix que l’on peut espérer réduire durablement la morbidité et briser le cycle de transmission.
Conclusion
A l’issue de cette étude menée auprès de 316 prestataires soignants confondus de la zone de santé rurale d’Oicha, une étude portant sur la prise en charge de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha, une étude transversale descriptive qui s’était déroulée durant 6 mois pour une période allant du 1er janvier au 30 juin 2024.L’étude de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha a permis de mettre en lumière la persistance de cette parasitose comme un problème de santé publique. Cette affection, liée à des conditions environnementales propices à la transmission et à des pratiques communautaires à risque, touche principalement les enfants d’âge scolaire et les populations vivant au contact des eaux douces contaminées.
Les résultats montrent que malgré les efforts de lutte déployés à travers les campagnes de traitement de masse au Praziquantel, la prévalence reste élevée dans certaines localités, en raison de multiples facteurs : accès insuffisant à l’eau potable, absence de latrines, faible sensibilisation des populations, couverture thérapeutique incomplète, et manque de suivi post-traitement. De plus, la capacité des structures sanitaires à assurer un dépistage systématique et une prise en charge continue des cas reste limitée. Pour répondre efficacement à cette problématique, il est essentiel d’adopter une approche intégrée et durable, combinant le traitement médical, amélioration des conditions d’hygiène et d’assainissement, éducation sanitaire, contrôle des mollusques vecteurs, et implication active de la communauté. La bilharziose à Schistosoma mansoni ne pourra être maîtrisée que par des actions coordonnées, adaptées au contexte local et soutenues à long terme, une analyse univariée était faite dans notre étude.
Références
- Chitsulo, L., Engels, D., Montresor, A., & Savioli, L. The global status of schistosomiasis and its control, 2000, Acta Tropica, 77(1), 41–51.
- Ross, A.G.P., et al. Advances in schistosomiasis vaccine development. Human Vaccines & Immunotherapeutics,2022, 18(5), 2041904.
DOI : 10.1080/21645515.2022.2041904 - Marc Gentilini, medecine tropicale,Medecine sciences,2012, P359-379,SBN 978-257-20396-0,6ème éd, Paris.
- Epilly trop,maladies infectieuses tropicales,CMIT,2022,P 52.
- Jan Clerinx, Alfons Van Gompel, Schistosomiasis in traveller’s and migrants, Travel Medicine and Infectious Disease, 2011, P 6–15
DOI : 10.1016/j.tmaid.2010.11.0011. - Oliosi E., Angoulvant A.,and al., Chronic schistosomiasis imported in France: A retrospective multicenter analysis of 532 patients, calling for international recommendations, Travel Medicine and Infectious Disease, 2023, DOI : 10.1016/j.tmaid.2023.102644, Pays-Bas.
- Allen G.P. Ross, Remigio M. and al., Road to the elimination of schistosomiasis from Asia: the journey is far from over, Microbes and Infection, Pages : 858–865, DOI : 10.1016/j.micinf.2013.07.010, France
- Kabuyaya, M., and al., Efficacy of praziquantel treatment regimens in pre-school and school aged children infected with schistosomes in sub-Saharan Africa: a systematic review, Infectious Diseases of Poverty, 2018, DOI : 10.1186/s40249-018-0448-x, Royaume-Uni
- Bruno Senghor, Souleymane Doucouré, Cheikh Sokhna, Urogenital schistosomiasis in three different water access in the Senegal river basin: prevalence and monitoring praziquantel efficacy and re-infection levels, BMC Infectious Diseases, 2022, DOI : 10.1186/s12879-022-07813-5, Royaume-Uni
- Ambe Fabrice Ngwa, Pride Tanyi Bobga, Ekwi Damian Nsongmayi, Gedeon Schadrack Yememe Yememe, Judith Ngong Nyeme, Mohamed Isah, Ebai Christabel Ashu, Calvin Bisong Ebai, Prevalence and Predictors Associated to Schistosoma mansoni Infection among Patients Attending the Saint Jean de Malte Hospital, Njombe, Littoral Region, Cameroon, Journal of Parasitology Research, 2023, DOI : 10.1155/2023/8674934, Royaume-Uni
- Ahmed M. Hussein and al., The Prevalence of Schistosomiasis among People in Almatama locality River Nile State, Sudan, Journal of Clinical Research in HIV/AIDS and Prevention, 2019, Pages : 1–6, DOI : 10.14302/issn.2324-7339.jcrhap-19-2711, États-Unis
- Onkanga, Isaac O.; Mwinzi and al., Impact of two rounds of praziquantel mass drug administration on Schistosoma mansoni infection prevalence and intensity: a comparison between community-wide treatment and school-based treatment in western Kenya, International Journal for Parasitology, 2016
P 439–445, DOI : 10.1016/j.ijpara.2016.01.006, Pays-Bas - Auteurs : Kabatereine and al., Efficacy and side effects of praziquantel treatment in a highly endemic Schistosoma mansoni focus at Lake Albert, Uganda, Transactions of the Royal Society of Tropical Medicine and Hygiene, 2003, P599–603, DOI : 10.1016/S0035-9203(03)80044-5, Royaume-Uni
- Kinunghi, Safari and al., Comparison of the Impact of Different Mass Drug Administration Strategies on Infection with Schistosoma mansoni in Mwanza Region, Tanzania—A Cluster-Randomized Controlled Trial, The American Journal of Tropical Medicine and Hygiene, 2018, 99(6) Pages : 1298–1306
DOI : 10.4269/ajtmh.18-0356, États-Unis - D. Engels, J. Ndoricimpa, B. Gryseels, Schistosomiasis mansoni in Burundi: progress in its control since 1985, Bulletin of the World Health Organization, 1993, 71(2), P 207–214, DOI : 10.2471/BLT.93.020207, Suisse
- Niyonzima, N. and al., Efficacy of Single-Dose Praziquantel for the Treatment of Schistosoma mansoni Infections among School Children in Rwanda, Journal of Tropical Medicine, 2023, 2023, DOI : 10.1155/2023/37764978, États-Unis
- Maurice M. Nigo and al., Epidemiology of Schistosoma mansoni infection in Ituri Province, North-eastern Democratic Republic of the Congo, medRxiv, 2020, DOI : 10.1101/2020.08.10.20171090
- Matangila and al., Malaria, schistosomiasis and soil transmitted helminth burden and their correlation with anemia in children attending primary schools in Kinshasa, Democratic Republic of Congo, PLoS ONE, 2014, 9(11), DOI : 10.1371/journal.pone.0110789, États-Unis
- Auteur : J. Schwetz, Note préliminaire sur la bilharziose à Sakania (Katanga, Congo Belge), Annales de la Société Belge de Médecine Tropicale, 1951, 3(1), P93–102, DOI : 10.1051/parasite/1951264323, Belgique.
- R. Khonde Kumbu, K. Mbanzulu Makola, Lu Bin, Prevalence of Schistosoma mansoni Infection in Four Health Areas of Kisantu Health Zone, Democratic Republic of the Congo, Advances in Medicine, 2016, DOI : 10.1155/2016/6596095, États-Unis
- Polderman, A. M.; Mpamila, K.; Manshande,On the distribution and control of schistosomiasis mansoni in Maniema, Zaire, Acta Leiden, 1982, (49), P17–29, DOI : 10.17058/acta.leiden.1982.49.1.17, Pays-Bas
- Hermès Mushayuma Namegabe, Étude d’impact de la variabilité climatique sur la schistosomiase dans la zone de santé de Katana, Sud-Kivu en RDC, 2008
Lieu de publication : Université ouverte campus de Bukavu
DOI : Non disponible, Lien : Accéder au mémoirehnjournal.net+3 - Astrid M. Knoblauch and al., Schistosomiasis and soil-transmitted helminth infections in schoolchildren in north-eastern Democratic Republic of the Congo, Transactions of The Royal Society of Tropical Medicine and Hygiene, 2016 ,110 (7), P424–426 ; DOI : 10.1093/trstmh/trw040, Royaume-Uni.
- Maurice M. Nigo and al., Epidemiology of Schistosoma mansoni infection in Ituri Province, North-eastern Democratic Republic of the Congo, PLOS Neglected Tropical Diseases, 2021, 15(12), DOI : 10.1371/journal.pntd.0009486, États-Unis.
- PNLMTN / Ministère de la Santé (RD Congo, Sénégal, Bénin, etc.) : Programmes nationaux de lutte contre les maladies tropicales négligées — rapports et plans stratégiques.
- BCZ OICHA, rapport annuel, 2023.

