Modélisation épidemiologique spatiale de la bilharziose à Schistosoma mansoni à partir des données de l’incidence de la dernière décennie dans la zone de santé rurale d’Oicha au Nord Kivu en RD Congo
Spatial Epidemiological Modeling of Schistosomiasis (Schistosoma mansoni) Based on Incidence Data from the Last Decade in the Rural Health Zone of Oicha, North Kivu, DR Congo
Bailanda Mumbere Pascal 1,2,6, Kahindo Nzalamingi Anselme5, Kimbilwa Katavali Emery7, Kakule Kithanga Jean de Dieu7, Kambale Mbakwiravyo Obede5, Mumbere Muvunga Shukuru5, Kule Kyusa Archip7, Nzanzu Ndulutulu Joachin 7, Kambale Soheranda Sadraka7, Manwa Budwaga Baudouin4, Wembo Ndeo Oscar3, Barhwamire Kabesha Theophile4, Muhindo Sahani Walere2, Paluku Sabuni Louis 3
1.Université Officielle de Semuliki de Beni, République Démocratique du Congo
2. Université Catholique du Graben de Butembo, République Démocratique du Congo
3.Université Officielle de Ruwenzori de Butembo, République Démocratique du Congo
4.Université officielle de Bukavu, République Démocratique du Congo
5.Instittut Supérieur Pédagogique d’Oicha, République Démocratique du Congo
6.Centre Hospitalier le Rocher d’Oicha, République Démocratique du Congo.
7.Zone de santé rurale d’Oicha, République Démocratique du Congo.
Auteur correspondant : drbailanda1@gmail.com
DOI: https://doi.org/10.53796/hnsj611/18
Identifiant de recherche scientifique arabe: https://arsri.org/10000/611/18
Volume (6) Numéro (11). Pages: 319 - 331
Reçu le: 2025-10-07 | Accepté le: 2025-10-15 | Publié le: 2025-11-01
Résumé: Introduction : La bilharziose, ou schistosomiase, constitue l'une des maladies parasitaires les plus importantes en termes de morbidité dans les régions tropicales et subtropicales. Elle est causée par des vers plats du genre Schistosoma, dont Schistosoma mansoni responsable de la forme intestinale. La modélisation épidémiologique spatiale s’impose aujourd’hui comme un outil précieux pour mieux comprendre, prédire et visualiser la dynamique de transmission de la bilharziose dans l’espace et le temps. L’objectif de l’étude était d’évaluer l’évolution spatio-temporelle de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha, en utilisant les données de prévalence de la dernière décennie et la méthode du rapport à la tendance, afin d’identifier les foyers de transmission persistants et d’orienter les interventions de contrôle de manière ciblée. Matériel et méthodes : Il s’agissait d’une étude épidémiologique spatiale sur les habitants de la zone de santé d’Oicha dont les données épidémiologiques humaines de l’incidence de la décennie (2015-2024) étaient chiffrées à 4 731, récoltées durant deux mois, soit du 1er Janvier au 1er mars 2025 ; sélectionnées et extraites à partir des canevas du Système National d’Information Sanitaire (SNIS) en utilisant une approche d’échantillonnage exhaustif des enregistrements disponibles pour la zone de santé rurale d’Oicha. Résultats : Les périodes à risque étaient en 2016, 2020 et 2023 ; les périodes où l’incidence avaient diminué : 2018, 2022 et 2024. La variable aléatoire normale réduite vaut : Z=0,2399⁄√0,00231=4,9914, et donc P(Z≥4,9914)=0,000. Le coefficient kappa de Cohen est très hautement significatif. Le classement, qui donne lieu à un léger accord, n’est donc pas l’effet du hasard. Les limites de confiance du Kappa ainsi estimé, au seuil de signification α=0,05, sont 0,2399±1,96√0,00231, soit 0,146 et 0,334. L’incidence de la bilharziose à S. mansoni est fortement influencée par les conditions écologiques des mollusques vecteurs. Conclusion : La modélisation épidémiologique spatiale constitue un outil précieux pour la planification et l’orientation des programmes de contrôle, en permettant de prioriser les aires de santé les plus vulnérables et d’optimiser l’allocation des ressources. Elle met en évidence la nécessité d’une approche intégrée associant interventions médicales, environnementales et communautaires pour réduire durablement la charge de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha.
Mots-clés: Modélisation épidemiologique, Bilharziose, incidence, décennie, ZSR Oicha.
Abstract: Introduction: Schistosomiasis, or bilharzia, is one of the most important parasitic diseases in terms of morbidity in tropical and subtropical regions. It is caused by flatworms of the genus Schistosoma, including Schistosoma mansoni, which is responsible for the intestinal form. Spatial epidemiological modeling has emerged as a valuable tool to better understand, predict, and visualize the transmission dynamics of bilharzia in space and time. The objective of this study was to assess the spatiotemporal evolution of Schistosoma mansoni bilharzia in the rural health zone of Oicha, using prevalence data from the last decade and the trend ratio method, in order to identify persistent transmission foci and guide targeted control interventions. Material and methods: This was a spatial epidemiological study on the inhabitants of the Oicha health zone whose human epidemiological incidence data for the decade (2015-2024) were estimated at 4,731, collected over two months, from January 1 to March 1, 2025; selected and extracted from the National Health Information System (SNIS) framework using an exhaustive sampling approach of the records available for the rural health zone of Oicha. Results: The risk periods were in 2016, 2020 and 2023; the periods where the prevalence had decreased: 2018, 2022 and 2024. The reduced normal random variable is: Z=0.2399⁄√0.00231=4.9914, and therefore P(Z≥4.9914) =0.000. Cohen's kappa coefficient is very highly significant. The ranking, which gives rise to a slight agreement, is therefore not the effect of chance. The confidence limits of the Kappa thus estimated, at the significance threshold α=0.05, are 0.2399±1.96√0.00231, or 0.146 and 0.334. The incidence of S. mansoni bilharzia is strongly influenced by the ecological conditions of the vector mollusks. Conclusion: Spatial epidemiological modeling is a valuable tool for planning and guiding control programs, enabling the prioritization of the most vulnerable health areas and optimizing resource allocation. It highlights the need for an integrated approach combining medical, environmental, and community interventions to sustainably reduce the burden of Schistosoma mansoni bilharzia in the Oicha rural health zone.
Keywords: Epidemiological modeling, Schistosomiasis, incidence, decade, Oicha SRZ.
1.Introduction
La bilharziose, ou schistosomiase, constitue l’une des maladies parasitaires les plus importantes en termes de morbidité dans les régions tropicales et subtropicales. Elle est causée par des vers plats du genre Schistosoma, dont Schistosoma mansoni responsable de la forme intestinale. La transmission de cette parasitose est étroitement liée à des facteurs environnementaux, sociaux et comportementaux, notamment la présence de plans d’eau douce infestés par des mollusques du genre Biomphalaria. La modélisation épidémiologique spatiale s’impose aujourd’hui comme un outil précieux pour mieux comprendre, prédire et visualiser la dynamique de transmission de la bilharziose dans l’espace et le temps. En intégrant les données épidémiologiques (prévalence, intensité d’infection), écologiques (température, végétation, précipitations, hydrologie), géographiques (coordonnées GPS, proximité des rivières ou marécages), et sociales (pratiques de contact avec l’eau) [1].
En France, bien que la bilharziose soit historiquement considérée comme une maladie tropicale, la découverte de foyers autochtones de Schistosoma en Corse depuis 2013, et les flux migratoires en provenance de zones endémiques d’Afrique subsaharienne, soulèvent de nouvelles préoccupations de santé publique en France métropolitaine et dans les territoires d’outre-mer. Dans ce contexte, Schistosoma mansoni devient une espèce d’intérêt, notamment dans les territoires ultramarins français, où des cas autochtones ont été recensés [2].
En Angleterre, la bilharziose à Schistosoma mansoni, n’est pas une maladie endémique. Toutefois, le pays est confronté à une augmentation notable de cas importés, principalement chez les migrants, réfugiés, demandeurs d’asile et voyageurs revenant d’Afrique subsaharienne. Ces cas sont souvent asymptomatiques ou sous-diagnostiqués, ce qui représente un défi pour les services de santé peu familiarisés avec cette parasitose. Les patients infectés par S. mansoni arrivent majoritairement de zones endémiques comme l’Érythrée, l’Éthiopie, le Nigeria ou le Soudan. Or, le NHS (National Health Service) ne dispose pas d’un système de surveillance systématique de la schistosomiase, et les cas sont souvent identifiés de manière opportuniste dans les services de maladies infectieuses [3,4].
Le Canada a connu une augmentation significative du nombre de cas importés de la bilharziose à Schistosoma mansoni, en lien avec l’immigration en provenance de zones endémiques ainsi que les voyages internationaux. Le système de santé canadien, bien qu’avancé, est confronté à des défis en matière de diagnostic précoce, de sensibilisation des professionnels de santé, et de suivi spatial des cas de la maladie à Schistosoma, qui restent souvent sous-déclarés ou détectés tardivement. Ces limites compromettent l’identification des foyers d’exposition à l’étranger, et la prise en charge ciblée dans les communautés à risque. La modélisation épidémiologique spatiale s’impose comme un outil essentiel pour cartographier la répartition spatiale des cas importés à l’échelle locale, pour identifier les zones de concentration de populations migrantes exposées dans leur pays d’origine et aider à la planification des stratégies de dépistage et de sensibilisation, dans une optique de santé publique préventive [5].
L’Australie est concerné par un nombre croissant de cas importés de bilharziose liés aux mouvements migratoires, aux voyages internationaux, et à la présence d’une diaspora provenant de zones endémiques, notamment d’Afrique et d’Amérique latine. Ces cas représentent un enjeu de santé publique émergent, principalement en termes de diagnostic précoce, prise en charge clinique et surveillance épidémiologique. La diversité géographique du pays, ainsi que ses vastes zones rurales et urbaines, rendent la compréhension spatiale des cas importés et des populations à risque essentielle. Par ailleurs, les conditions écologiques australiennes ne favorisent pas la survie des mollusques hôtes nécessaires à la transmission locale, ce qui limite le risque d’émergence autochtone. L’utilisation des systèmes d’information géographique (SIG), couplée à des modèles statistiques avancés (modèles bayésiens, apprentissage automatique), permettrait d’améliorer la cartographie de la maladie, d’identifier les facteurs de risque environnementaux et sociaux, et d’accompagner la prise de décision sanitaire [6].
Au Sénégal, la bilharziose à Schistosoma mansoni demeure une maladie parasitaire endémique, particulièrement dans les zones de la vallée du fleuve Sénégal, du delta du Saloum, et certaines régions du sud-est. La persistance et la variabilité spatiale de la maladie sont influencées par plusieurs facteurs écologiques, sociaux et hydrologiques, notamment la présence de mollusques hôtes, les pratiques agricoles et la distribution des populations humaines. La lutte contre la bilharziose au Sénégal est confrontée à des défis majeurs, dont la variabilité spatiale importante de la transmission, la réapparition de foyers malgré les campagnes de traitement, ainsi que les effets des modifications environnementales liées aux aménagements hydro-agricoles et aux changements climatiques. L’intégration des technologies modernes de télédétection, des systèmes d’information géographique (SIG) et des modèles statistiques avancés (comme les modèles bayésiens spatiaux) est essentielle pour une surveillance efficace et une prise de décision éclairée dans le cadre des programmes nationaux de lutte [7].
En Afrique du Sud, la bilharziose à Schistosoma mansoni est une maladie parasitaire d’importance variable selon les régions, avec une distribution focalisée principalement dans les provinces du KwaZulu-Natal, du Limpopo et du Mpumalanga. Les conditions écologiques, notamment la présence de milieux aquatiques propices aux mollusques vecteurs, ainsi que les activités humaines (agriculture, pêche, utilisation domestique de l’eau), influencent fortement la dynamique spatiale de la transmission. La maladie demeure un problème de santé publique, en particulier dans les zones rurales défavorisées où l’accès à l’eau potable et aux installations sanitaires est limité. Malgré les efforts de contrôle, la persistance et la variabilité spatiale des foyers infectieux compliquent la lutte. La modélisation épidémiologique spatiale est un outil essentiel pour comprendre la distribution géographique de la maladie, identifier les zones à risque élevé, et guider les interventions ciblées. Elle permet d’intégrer divers types de données climatiques, environnementales, sociales et démographiques pour mieux prédire les schémas de transmission [8].
Au Kenya, la bilharziose à Schistosoma mansoni constitue une importante maladie parasitaire à transmission focalisée, principalement dans les régions riveraines du lac Victoria, du lac Baringo, ainsi que dans certaines zones du Rift Valley et des régions côtières. La transmission est fortement influencée par la présence d’hôtes intermédiaires mollusques (Biomphalaria) et par les interactions entre les pratiques agricoles, l’accès à l’eau, et les comportements humains. La variabilité spatiale et temporelle de la maladie est marquée, avec des zones de haute prévalence coexistant avec des régions où la maladie est absente ou sporadique. Cette hétérogénéité rend les interventions de contrôle complexes et nécessite une compréhension fine des déterminants locaux. La modélisation fait face à des défis, notamment la qualité et la disponibilité des données, la complexité des interactions écologiques, et la nécessité d’adapter les modèles aux réalités locales pour une application efficace dans la planification sanitaire [9].
En RD Congo, La bilharziose intestinale causée par Schistosoma mansoni constitue un problème majeur de santé publique en République Démocratique du Congo, particulièrement dans les zones rurales et périurbaines le long des systèmes hydrographiques (rivières, marais, canaux). La prévalence de la maladie reste élevée dans plusieurs provinces, notamment celles du Nord-Kivu, du Sud-Kivu, de la Tshopo, du Kasaï et de l’Ituri. Malgré les campagnes de traitement de masse par le praziquantel, la persistance des foyers de transmission révèle des lacunes dans la surveillance, la cartographie précise et la compréhension des dynamiques locales de transmission. Cependant, en RDC, l’approche de la modélisation épidemiologique spatiale reste encore peu développée, notamment à cause de la disponibilité limitée des données géoréférencées, du manque d’outils d’analyse spatiale à l’échelle locale, et d’une faible intégration des données écologiques, démographiques et sanitaires dans les modèles prédictifs [10,11].
A Kinshasa, La bilharziose intestinale due à Schistosoma mansoni est une maladie parasitaire à transmission hydrique qui reste un défi de santé publique à Kinshasa, malgré son statut urbain. La ville, traversée par plusieurs cours d’eau, rivières et canaux, ainsi que par le fleuve Congo, présente des zones d’endémie souvent méconnues ou sous-estimées, en raison de la forte urbanisation et de la disparité des conditions sanitaires. Le principal problème est que la transmission est fortement localisée autour des milieux aquatiques stagnants ou lentement courants, où les hôtes intermédiaires (escargots du genre Biomphalaria) trouvent un environnement favorable. La variabilité écologique dans une métropole aussi vaste et diverse que Kinshasa génère une hétérogénéité spatiale marquée de la transmission, allant de zones urbaines à faible risque à des poches endémiques persistantes dans les quartiers périphériques, les marécages et les zones à faible assainissement. Cependant, la modélisation épidémiologique spatiale reste encore insuffisamment développée à Kinshasa, en raison notamment : du manque de données systématiques géoréférencées à l’échelle intra-urbaine, des difficultés d’intégrer la diversité des milieux hydrologiques urbains, des contraintes liées aux mobilités humaines et aux dynamiques urbaines complexes et du peu de recours aux techniques avancées comme les SIG et les modèles bayésiens dans les études locales. Cette situation limite la capacité des autorités sanitaires à identifier précisément les zones à haut risque, à prioriser les interventions (notamment les campagnes de distribution de praziquantel) et à mettre en place une surveillance efficace pour prévenir la réémergence [12].
En Ituri, une région forestière du nord-est de la République Démocratique du Congo, est une zone d’endémie reconnue pour la bilharziose intestinale causée par Schistosoma mansoni. La prévalence y est souvent élevée, avec des foyers concentrés autour des cours d’eau, rivières et zones marécageuses où les escargots vecteurs (Biomphalaria) prolifèrent. Cependant, la région est caractérisée par une grande hétérogénéité spatiale liée à sa diversité écologique, ses infrastructures limitées et ses dynamiques humaines complexes. La modélisation épidémiologique spatiale de la bilharziose à S. mansoni en Ituri devrait viser à comprendre cette variabilité locale de la transmission pour identifier précisément les hotspots à risque élevé, souvent dispersés et parfois isolés, dans un territoire difficile d’accès, intégrer les facteurs environnementaux (température, humidité, végétation, hydrographie) et socio-économiques (accès à l’eau potable, assainissement, pratiques agricoles) qui influencent la répartition des infections [13].
La province du Sud-Kivu, située dans l’Est de la République Démocratique du Congo, est une zone reconnue pour la prévalence élevée de la bilharziose intestinale à Schistosoma mansoni. Cette région est caractérisée par une topographie variée incluant des hauts plateaux, des vallées et des cours d’eau majeurs (notamment la rivière Ruzizi, le lac Kivu et plusieurs affluents), créant ainsi des milieux favorables à la survie des escargots vecteurs du genre Biomphalaria. La transmission de la bilharziose y est fortement focalisée et varie d’un micro-territoire à un autre en fonction des facteurs écologiques (présence d’eau stagnante, température, végétation), socio-économiques (accès à l’eau potable, pratiques agricoles) et démographiques (densité de population, mobilité). Cette hétérogénéité spatiale rend difficile la planification d’interventions de santé publique efficaces sans une compréhension fine de la dynamique locale de transmission. La modélisation épidémiologique spatiale est donc essentielle pour cartographier précisément les foyers à haut risque, intégrer des données écologiques, climatiques et démographiques pour expliquer les variations spatiales, suivre l’évolution temporelle de la transmission dans un contexte marqué par les déplacements de population liés aux conflits et aux activités économiques et optimiser le ciblage des campagnes de traitement de masse par praziquantel pour une meilleure efficacité [14].
La province du Nord-Kivu, située à l’est de la République Démocratique du Congo, est aussi une zone endémique pour la bilharziose intestinale causée par Schistosoma mansoni. La région est traversée par plusieurs cours d’eau, rivières et lacs, notamment le lac Édouard, qui constituent des habitats favorables aux escargots vecteurs (Biomphalaria), vecteurs indispensables à la transmission du parasite. La transmission de la bilharziose y est fortement influencée par les caractéristiques environnementales et hydrologiques, ainsi que par les activités humaines telles que l’agriculture, la pêche, et l’accès limité à l’eau potable et à l’assainissement. La modélisation épidémiologique spatiale est essentielle pour cartographier les foyers de transmission et identifier les zones à risque élevé, intégrer les données écologiques, hydrologiques et démographiques pour mieux comprendre la répartition spatiale, prédire les zones où les interventions de la santé publique seront les plus efficaces et surveiller l’évolution temporelle des foyers de transmission dans un contexte marqué par les déplacements humains [15, 16].
La zone de santé rurale d’Oicha, située dans la province du Nord-Kivu en République Démocratique du Congo, est une région où la bilharziose intestinale à Schistosoma mansoni est endémique. Cette zone est caractérisée par un environnement tropical humide, marqué par la présence de nombreux cours d’eau, rivières et marécages, favorables au développement des escargots vecteurs du genre Biomphalaria. La transmission de la bilharziose y est influencée par plusieurs facteurs environnementaux et socio-économiques , la proximité des populations avec les sources d’eau douce stagnante ou à faible courant, les activités humaines telles que l’agriculture, la pêche et la collecte d’eau pour usage domestique, les conditions sanitaires souvent précaires, notamment l’accès limité à l’eau potable et aux installations d’assainissement et les déplacements de population dus aux conflits et instabilités dans la région, qui peuvent modifier la dynamique de transmission. La modélisation quasi absente rencontre plusieurs défis dans la zone de santé rurale d’Oicha : la disponibilité limitée de données précises et actualisées, notamment en raison des difficultés d’accès et du contexte sécuritaire fragile, la complexité des interactions entre facteurs naturels et humains qui influencent la transmission et la nécessité données.
La question principale de l’étude était de savoir l’évolution spatio-temporelle de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha au cours de la dernière décennie et quels sont les foyers de transmission persistants identifiables à partir des données de l’incidence. L’hypothèse principale est que l’incidence de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha a augmenté au cours de la dernière décennie, les foyers de transmission persistants subsistent, pouvant être identifiés grâce à la modélisation spatiale et à la méthode du rapport à la tendance.
Objectif général
Évaluer l’évolution spatio-temporelle de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha, en utilisant les données de l’incidence de la dernière décennie et la méthode du rapport à la tendance, afin d’identifier les foyers de transmission persistants et d’orienter les interventions de contrôle de manière ciblée.
Objectifs spécifiques
1.Évaluer le niveau de concordance entre les résultats des deux laboratoires à l’aide du coefficient Kappa, afin d’apprécier la fiabilité, la reproductibilité et la validité des tests réalisés sur les mêmes échantillons.
2. Analyser l’incidence de la bilharziose à Schistosoma mansoni et les paramètres écologiques des mollusques.
2.Matériel et méthodes
2.1. Cadre de l’étude
Notre étude était menée dans la zone de santé rurale d’Oicha se situant dans le Territoire de Beni au Nord Kivu en République Démocratique du Congo, couvre une superficie de 1.656 Km2, située latitude Est 77696,989 m, longitude Nord 780671,652 m, altitude 1050,9 m avec une précision de 1,5 m et une population de 341.730 habitants répartis dans 27 aires de santé.
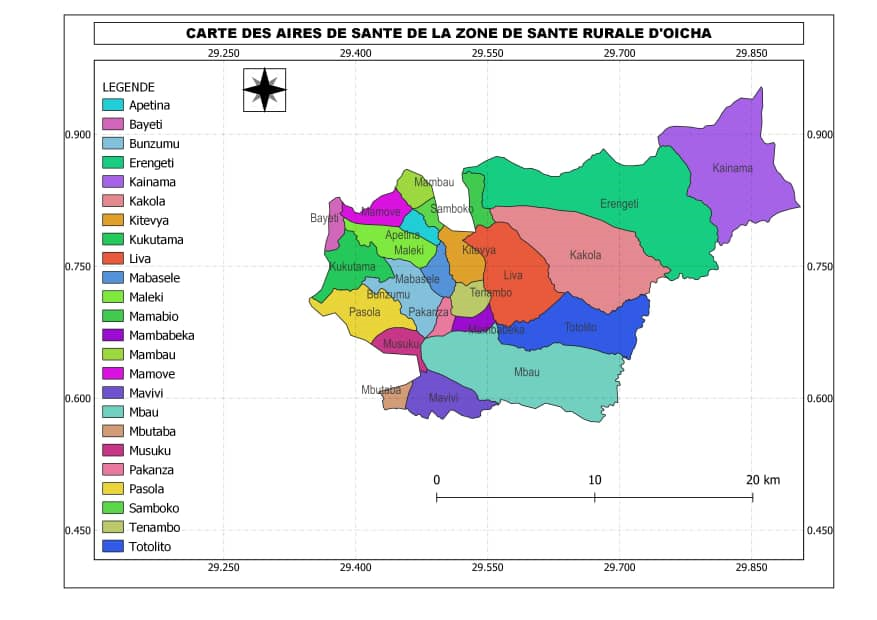
Figure 1. Carte postale de la zone de santé rurale d’Oicha.
2.2.Type d’étude
Il s’agissait d’une étude épidémiologique spatiale.
2.3. Variables d’étude
Les variables indépendantes : les facteurs environnementaux et écologiques, socio comportementaux, liés aux interventions de la santé publique, temporels et géographiques.
La variable dépendante : la bilharziose à Schistosoma mansoni.
2.4. Population, taille et période d’étude
La population d’étude comprenait les habitants de la zone de santé rurale d’Oicha dont les données épidémiologiques humaines de l’incidence de la décennie (2015-2024) étaient chiffrées à 4 731, récoltées durant deux mois, soit du 1er Janvier au 1er mars 2025.
2.5. Technique d’échantillonnage des données
Les données de la décennie ont été sélectionnées et extraites à partir des canevas du Système National d’Information Sanitaire (SNIS) en utilisant une approche d’échantillonnage exhaustif des enregistrements disponibles pour la zone de santé rurale d’Oicha. Cette méthode avait permis de prendre en compte toutes les informations pertinentes sur l’incidence de la bilharziose à Schistosoma mansoni enregistrées au cours des dix dernières années, tout en garantissant la représentativité des données pour l’analyse spatio-temporelle.
2.6. Critères d’éligibilité
Les critères d’inclusion : Les données de la bilharziose à S. mansoni récoltées dans les laboratoires des formations sanitaires de la zone de santé rurale d’Oicha, les données de l’incidence de la décennie se trouvant dans les canevas de SNIS bien rempli, les données écologiques des mollusques hôtes intermédiaires récoltées dans les rivières de la zone de santé rurale d’Oicha.
Les critères de non inclusion : tous les cas venus en dehors de la zone de santé, toutes les données mal enregistrées dans les canevas de SNIS, les étangs, les marées.
2.7. Collecte, analyse et traitement des données
Nous avions collecté rigoureusement les données d’une décennie (2015-2024) sur la bilharziose à Schistosoma mansoni dans les registres, correctement enregistrées. Leur nettoyage, transcription par le logiciel Word 2010, leurs analyses étaient faites à l’aide du logiciel R ; qui avait permis de prédire la dynamique spatiale de transmission et de guider les interventions de santé publique dans l’avenir.
2.8. Considérations éthiques
L’étude avait obtenu une autorisation du comité d’éthique médicale de l’Université de Goma, en République Démocratique du Congo par l’attestation N° Approbation : UNIGOM/CEM/010/2023 du 01 Mars 2023. Nous avions contacté les autorités politico administratives locales pour visa et autorisation de l’étude dans la zone de santé rurale d’Oicha.
L’étude était menée dans l’intégrité, la discrétion et confidentialité des données récoltées.
3.Résultats
I. Méthodes de mesure des variations saisonnières de la bilharziose à Schistosoma mansoni.
Tableau 1. Méthode du rapport à la tendance
|
ANNEE |
T1 |
T2 |
T3 |
T4 |
TOTAUX |
(X) |
Moyenne trimestrielle (y) |
ya+bx |
||
|
2015 |
67 |
55 |
49 |
74 |
245 |
-5 |
61,25 |
-306,25 |
25 |
125,1 |
|
2016 |
102 |
97 |
66 |
70 |
335 |
-4 |
83,75 |
-335 |
16 |
123,975 |
|
2017 |
111 |
227 |
139 |
128 |
605 |
-3 |
151,25 |
-453,75 |
9 |
122,85 |
|
2018 |
92 |
168 |
336 |
407 |
1003 |
-2 |
250,75 |
-501,5 |
4 |
121,725 |
|
2019 |
166 |
146 |
125 |
88 |
525 |
-1 |
131,25 |
-131,25 |
1 |
120,6 |
|
2020 |
70 |
111 |
83 |
74 |
338 |
1 |
84,5 |
84,5 |
1 |
118,35 |
|
2021 |
89 |
109 |
128 |
135 |
461 |
2 |
115,25 |
230,5 |
4 |
117,225 |
|
2022 |
116 |
101 |
99 |
90 |
406 |
3 |
101,5 |
304,5 |
9 |
116,1 |
|
2023 |
95 |
89 |
72 |
111 |
367 |
4 |
91,75 |
367 |
16 |
114,975 |
|
2024 |
124 |
115 |
107 |
148 |
494 |
5 |
123,5 |
617,5 |
25 |
113,85 |
|
1194,75 |
-123,75 |
110 |
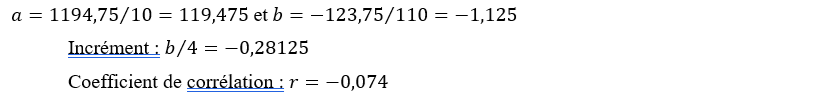
|
Valeurs observées en % des valeurs de tendance |
Valeurs observées en % des valeurs de tendance |
|||||||
|
T1 |
T2 |
T3 |
T4 |
T1 |
T2 |
T3 |
T4 |
|
|
125,522 |
125,241 |
124,959 |
124,678 |
53,38 |
43,92 |
39,21 |
59,35 |
|
|
124,397 |
124,116 |
123,834 |
123,553 |
82,00 |
78,15 |
53,30 |
56,66 |
|
|
123,272 |
122,991 |
122,709 |
122,428 |
90,04 |
184,57 |
113,28 |
104,55 |
|
|
122,147 |
121,866 |
121,584 |
121,303 |
75,32 |
137,86 |
276,35 |
335,52 |
|
|
121,022 |
120,741 |
120,459 |
120,178 |
137,17 |
120,92 |
103,77 |
73,22 |
|
|
118,772 |
118,491 |
118,209 |
117,928 |
58,94 |
93,68 |
70,21 |
62,75 |
|
|
117,647 |
117,366 |
117,084 |
116,803 |
75,65 |
92,87 |
109,32 |
115,58 |
|
|
116,522 |
116,241 |
115,959 |
115,678 |
99,55 |
86,89 |
85,37 |
77,80 |
|
|
115,397 |
115,116 |
114,834 |
114,553 |
82,32 |
77,31 |
62,70 |
96,90 |
|
|
114,272 |
113,991 |
113,709 |
113,428 |
108,51 |
100,89 |
94,10 |
130,48 |
|
|
Totaux |
862,88 |
1017,05 |
1007,62 |
1112,82 |
||||
|
Moyenne |
86,29 |
101,71 |
100,76 |
111,28 |
100,01 |
|||
|
Indice saisonnier |
86,28 |
101,70 |
100,75 |
111,27 |
||||
Le tableau 1 permet de visualiser les années critiques, la progression ou la diminution de la maladie, et de repérer les périodes d’augmentation ou de contrôle de l’infection.
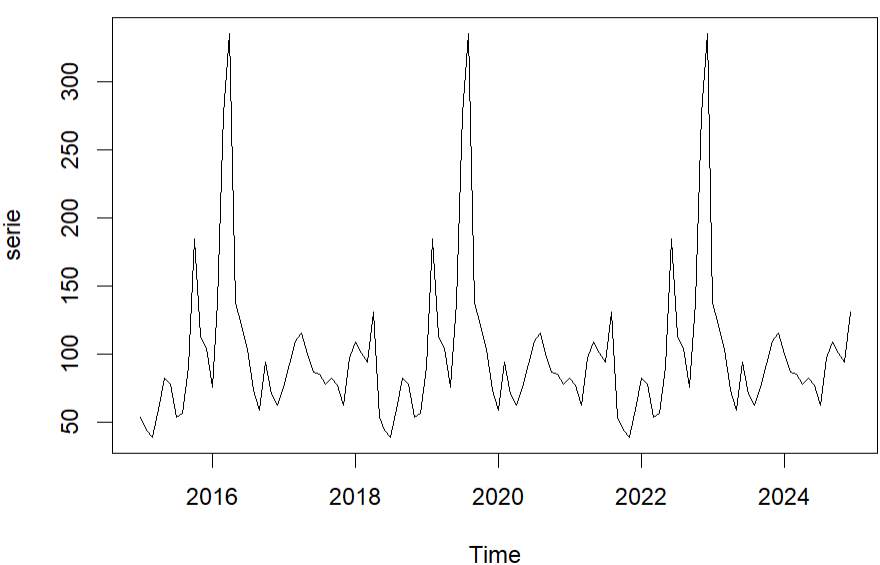
Figure 2. Diagramme évolutif trimestriel de la bilharziose intestinale : Méthode du rapport à la tendance.
La lecture de la figure 5 nous permet d’identifier les années avec une forte augmentation des cas ou périodes à risque élevé en 2016, 2020 et 2023 ; les périodes où la prévalence diminue 2018, 2022 et 2024, reflétant l’efficacité des interventions et les années de stabilité, indiquant un contrôle relatif de la maladie dans la zone de santé rurale d’Oicha.
II. Etude de la concordance des tests de la bilharziose à Schistosoma mansoni par deux laboratoires.
Tableau 2. Dépistage de la bilharziose à Schistosoma mansoni pour 400 échantillons par la méthode standard.
|
Test Kato-Katz / Kato-Katz |
Méthode classique de dépistage |
Totaux |
|
|
Test positif |
Test négatif |
||
|
Test positif Test négatif |
120 54 |
100 126 |
220 180 |
|
Totaux |
174 |
226 |
400 |
Le tableau 2, nous informe que deux laboratoires de dépistage de la bilharziose intestinale ont été utilisées sur 400 échantillons : la méthode Kato-Katz / Kato-Katz et la méthode classique. On se demande s’il y a concordance dans la classification par ces deux laboratoires autour de test ; le résultat obtenu et consigné dans le 2 laboratoires.
La variable étant catégorielle nominale, on peut bien faire le test de signification du coefficient kappa de Cohen, les valeurs estimées de et de étant respectivement égales à :


III. Incidence de la bilharziose à Schistosoma mansoni et les paramètres écologiques des mollusques.
Figure 3. Incidence de la bilharziose à Schistosoma mansoni et les paramètres écologiques des mollusques.
La figure 3 nous informe que l’incidence de la bilharziose à S. mansoni est fortement influencée par les conditions écologiques des mollusques vecteurs. Les interventions ciblant les sites à forte densité de mollusques ou les périodes où les conditions écologiques favorisent leur reproduction peuvent réduire efficacement la transmission. Le potentiel d’oxydoréduction de l’eau est inférieur à la valeur normale, cela prouve que l’eau des rivières est polluée dans la zone de santé rurale d’Oicha.
Discussion
La méthode du rapport à la tendance
Le tableau 1 permet de visualiser les années critiques, la progression ou la diminution de la maladie, et de repérer les périodes d’augmentation ou de contrôle de l’infection. Cette méthode du rapport à la tendance nous a permis d’intégrer et de synthétiser la série de l’incidence décennale en extrayant, année par année, en regroupant trimestriellement, la direction et l’amplitude des changements (variation annuelle) puis en caractérisant chaque segment temporel comme hausse, baisse ou stable. Cette approche, associée à la modélisation spatiale, nous a facilité une lecture opérationnelle des résultats qui correspondent aux résultats obtenus par BERRY A ET AL., MOUAHID G, SIMOONGA C, ETZINGER J, BROOKER S, VOUNATSOU P dans leurs recherches qui avaient identifié non seulement une tendance globale dans la zone de santé, mais aussi des disparités locales (poches endémiques, points chauds) et des périodes critiques.
Le diagramme évolutif trimestriel de la bilharziose intestinale
La lecture de la figure 5 nous a permis d’identifier les années avec une forte augmentation des cas ou périodes à risque élevé en 2016, 2020 et 2023 ; les périodes où la prévalence diminue 2018, 2022 et 2024, reflétant l’efficacité des interventions et les années de stabilité, indiquant un contrôle relatif de la maladie dans la zone de santé rurale d’Oicha. Le diagramme a montré une évolution globale marquée par une tendance à la baisse progressive de l’incidence dans la plupart des trimestres, traduisant un impact positif des interventions (traitements de masse, sensibilisation communautaire, amélioration de l’accès à l’eau potable). Toutefois, certains pics trimestriels récurrents persistent, ce qui indique la présence d’un cycle de transmission saisonnier non totalement maîtrisé. Les résultats montrent une augmentation des cas au cours des trimestres correspondant à la saison des pluies, où les rivières et points d’eau sont plus accessibles et fréquentés par la population pour les activités domestiques, agricoles ou récréatives. En revanche, une diminution relative est observée en saison sèche, période où les points d’eau sont moins nombreux et moins fréquentés. Cette variation saisonnière confirme les résultats obtenus par CLEMENTS ACA ET BROOKER RASO G, VOUNATSOU P, SINGER BH, N’GORAN ; l’influence directe des facteurs hydrologiques et écologiques sur la dynamique de la bilharziose intestinale. Malgré les fluctuations saisonnières, la comparaison des courbes trimestrielles d’une année à l’autre montre que les pics annuels tendent à être moins élevés au fil du temps, ce qui traduit une diminution de l’intensité de transmission. Le diagramme évolutif trimestriel révèle une baisse progressive de la bilharziose intestinale sur la décennie, tout en mettant en évidence des cycles saisonniers persistants et des disparités locales. Ces résultats orientent vers la nécessité de renforcer les interventions de manière ciblée, intégrée et saisonnièrement adaptée.
Le tableau 2, nous a informé que deux laboratoires de dépistage de la bilharziose intestinale ont été utilisées sur 400 échantillons : la méthode Kato-Katz / Kato-Katz et la méthode classique. On se demande s’il y a concordance dans la classification par ces deux laboratoires autour de test ; le résultat obtenu et consigné dans le 2 laboratoires.
La variable étant catégorielle nominale, on peut bien faire le test de signification du coefficient kappa de Cohen, les valeurs estimées de et de étant respectivement égales à :


Incidence de la bilharziose à Schistosoma mansoni et les paramètres écologiques des mollusques.
La figure 3 nous a informé que l’incidence de la bilharziose à S. mansoni est fortement influencée par les conditions écologiques des mollusques vecteurs. Les interventions ciblant les sites à forte densité de mollusques ou les périodes où les conditions écologiques favorisent leur reproduction peuvent réduire efficacement la transmission. Les résultats montrent une corrélation positive entre la densité des mollusques du genre Biomphalaria et l’incidence de la bilharziose. Dans les sites où la densité des mollusques était élevée, les taux d’incidence humaine se sont révélés significativement supérieurs. Cela confirme que la densité des mollusques constitue un facteur déterminant de la transmission, comme le rapportent des études similaires en Afrique subsaharienne par ONYEKACHI ESTHER NWOKO, TAWANDA MANYANGADZE ET MOSES JOHN CHIMBARI dans leur article “Spatial distribution, abondance, and infection rates of Human schistosome-transmitting snails and related physicochemical parameters in KwaZulu-Natal (KZN) province, South Africa”. L’influence des paramètres physico-chimiques de l’eau : température : une incidence plus élevée est observée dans les zones où la température de l’eau se situe entre 20 et 30 °C, gamme favorable à la survie et à la reproduction des mollusques ainsi qu’à la maturation des cercaires, le pH : des valeurs légèrement neutres à basiques ont coïncidé avec des foyers de transmission plus intense, reflétant l’optimum physiologique pour les mollusques, la turbidité et profondeur : une turbidité modérée et des eaux relativement stagnantes ont favorisé la concentration des mollusques et donc un risque accru de contamination humaine. L’influence des facteurs hydrologiques et saisonniers : l’incidence de la bilharziose présente une variabilité saisonnière, avec une augmentation pendant ou juste après la saison des pluies, période où les habitats des mollusques s’élargissent et où la fréquentation humaine des points d’eau est plus importante. Durant la saison sèche, une diminution relative des cas est observée, traduisant la contraction des habitats aquatiques. Pour la comparaison avec d’autres études : les tendances observées concordent avec les résultats rapportés dans d’autres contextes endémiques : plus la densité et l’infection des mollusques augmentent, plus l’incidence humaine s’élève. Cependant, la force de la corrélation peut varier selon la nature des points d’eau et le degré d’exposition communautaire ; ces résultats sont semblables à ceux trouvés par GAZZINELLI A, LOBATO L, MATOSO L, AVILA R. et NDEFFO MBAH ML, SKRIP LA, GALVANI AP.
Limites :1) les limites liées aux données : les données historiques incomplètes ou manquantes, la variabilité de la qualité des données.2) Limites méthodologiques : le modèle de modélisation spatiale : les modèles reposent sur des hypothèses (homogénéité de la population, distribution des vecteurs) qui peuvent simplifier la réalité. 3) Limites écologiques et environnementales : variabilité des paramètres environnementaux (pluviométrie, végétation aquatique) non intégrée ou mesurée approximativement. 4) Limites liées à la dynamique de la maladie :la prévalence observée reflète la transmission passée, pas nécessairement l’état actuel de la transmission.5) Limites analytiques : la corrélation entre prévalence humaine et la distribution des mollusques peut ne pas refléter une causalité directe.
Conclusion
L’analyse et la modélisation épidémiologique spatiale des données de l’incidence de la bilharziose intestinale au cours de la dernière décennie dans la zone de santé rurale d’Oicha montrent que cette parasitose demeure un problème majeur de santé publique. La cartographie spatiale révèle une distribution hétérogène de la maladie, fortement influencée par la proximité des points d’eau douce et la présence des mollusques vecteurs. L’évolution temporelle met en évidence des fluctuations liées aux conditions écologiques, aux variations climatiques, ainsi qu’aux pratiques humaines favorisant le contact avec l’eau contaminée. La méthode de modélisation spatiale avait permis d’identifier des aires de santé à haut risque, constituant des foyers endémiques persistants, où la transmission reste active malgré les efforts de lutte. Ces résultats avaient souligné l’importance de renforcer les interventions ciblées, telles que la chimio prévention de masse, l’amélioration de l’accès à l’eau potable et à l’assainissement, ainsi que la surveillance écologique des gîtes à mollusques.
En définitive, la modélisation épidémiologique spatiale constitue un outil précieux pour la planification et l’orientation des programmes de contrôle, en permettant de prioriser les aires de santé les plus vulnérables et d’optimiser l’allocation des ressources. Elle met en évidence la nécessité d’une approche intégrée associant interventions médicales, environnementales et communautaires pour réduire durablement la charge de la bilharziose à Schistosoma mansoni dans la zone de santé rurale d’Oicha.
Recommandations
Renforcement du contrôle médical, la surveillance et la recherche : Prioriser les zones à haut risque identifiées par la modélisation pour la chimio prévention de masse au praziquantel, assurer une couverture optimale des populations scolaires et des groupes les plus exposés et instituer un système de suivi épidémiologique et écologique régulier (incidence, densité des mollusques) et actualiser périodiquement les modèles spatiaux en intégrant les données climatiques, écologiques et comportementales.
Amélioration des conditions environnementales et WASH : développer l’accès à l’eau potable et aux infrastructures sanitaires et mettre en œuvre des actions de gestion écologique des gîtes de mollusques pour réduire la transmission.
Approche communautaire et multisectorielle : renforcer la sensibilisation et l’éducation sanitaire des communautés et promouvoir une collaboration intersectorielle (santé, eau, environnement, agriculture) pour une lutte durable.
Conflit d’Intérêt : Les auteurs ne déclarent aucun conflit d’intérêt par rapport à l’étude.
Contribution des auteurs
Bailanda Mumbere Pascal était l’auteur principal, avait conçu et piloté l’étude ,Paluku Sabuni Louis, Muhindo Sahani Walere, Barhwamire Kabesha Théophile, Wembo Ndeo Oscar, Manwa Budwaga Baudouin ont apprécié, orienté et supervisé le processus de recherche de l’étude ; plus de conseil Kambale Soheranda Sadraka, Kule Kyusa Archip, Nzanzu Nduluthulu Joachin, Kahindo Nzalamingi Anselme, Kimbilwa Katavali Emery, Kakule Kithanga Jean de Dieu, Kambale, Nzalamingi Anselme Mbakwiravyo Obede et Mumbere Muvunga Shukuru.
Conflit d’intérêt : Les auteurs ne déclarent aucun conflit d’intérêt par rapport à l’étude.
Financement : Cette étude n’avait reçu aucun financement externe.
Références
- Lai YS, Biedermann P, Ekpo UF, Garba A, Mathieu E, Midzi N, et al. Spatial distribution of schistosomiasis and treatment needs in sub-Saharan Africa: a systematic review and geostatistical analysis. Lancet Infect Dis. 2015;15(8):927–40.
Doi :10.1016/S1473-3099(15)00066-3 - Clements ACA, Brooker S. Epidemiological applications of geographical information systems: spatial analysis of helminth infections in Africa. Acta Trop. 2008 ;108(2-3):168–74.
Doi: 10.1016/j.actatropica.2008.09.001 - Sturrock HJW, Gething PW, Clements ACA, Brooker S. Optimal survey designs for targeting chemotherapy to control schistosomiasis in sub-Saharan Africa: a modelling study.ParasitVectors.2011;4:52.
Doi:10.1186/1756-3305-4-5 - Utzinger J, Raso G, Brooker S, De Savigny D, Tanner M, Ornbjerg N, et al. Schistosomiasis and neglected tropicaldiseases:towardsintegratedandsustainablecontrolandawordofcaution. Parasitology.2009;136(13):1859–74.
doi:10.1017/S0031182009991600 - Raso G, Vounatsou P, Singer BH, N’Goran EK, Tanner M, Utzinger J. An integrated approach for risk profiling and spatial prediction of Schistosoma mansoni-hookworm coinfection. Proc NatlAcad Sci U S A. 2006;103(18):6934–9.Doi :10.1073/pnas.0601553103
- Gazzinelli A, Lobato L, Matoso L, Avila R, Gazzinelli MF, Kloos H. Spatial distribution of Schistosoma mansoni infection before and after control activities in a rural area of northeastern Brazil. Mem Inst Oswaldo Cruz. 2006 ;101 Suppl 1:63–71. Doi :10.1590/S0074-02762006000900011
- Ndeffo Mbah ML, Skrip LA, Galvani AP. Improving spatial allocation of schistosomiasis treatment by geostatistical model-based decision making. PLoS Negl Trop Dis. 2014;8(9):e3136.
doi:10.1371/journal.pntd.0003136 - Raso G, Vounatsou P, Gosoniu L, Tanner M, N’Goran EK, Utzinger J. Risk factors and spatial patterns of hookworm infection among schoolchildren in a rural area of western Côted’Ivoire.IntJParasitol.2006;36(2):201–10.
doi:10.1016/j.ijpara.2005.09.009 - Simoonga C, Utzinger J, Brooker S, Vounatsou P, Appleton CC, Stensgaard AS, et al. Remote sensing, geographical information system and spatial analysis for schistosomiasis epidemiology and ecology in Africa.Parasitology.2009;136(13):1683–93.
doi:10.1017/S0031182009005998 - Soares Magalhães RJ, Barnett AG, Clements ACA. Geographical analysis of the role of water supply and sanitation in the risk of helminth infections of children in West Africa. Proc Natl Acad Sci U S A. 2011;108(50):20084–9.
doi:10.1073/pnas.1106784108 - Berry A, Moné H, Iriart X, Mouahid G, Aboo O, Boissier J. Schistosomiasis haematobium, Corsica, France. EmergInfectDis. 2014 ;20(9):1595–7.
doi:10.3201/eid2009.140928 - Boissier J, Grech-Angelini S, Webster BL, Allienne JF, Huyse T, Mas-Coma S, et al. Outbreak of urogenital schistosomiasis in Corsica (France): an epidemiological case study. Lancet Infect Dis. 2016 ;16(8) :971–9.
doi:10.1016/S1473-3099(16)00175-4 - Collinet-Adler S, Ward BJ, King CH. Schistosomiasis in travelers: a review of the literature and recommendations for management. Travel Med Infect Dis. 2016;14(3):243–52.
doi: 10.1016/j.tmaid.2016.04.005 - Simoonga C, Utzinger J, Brooker S, Vounatsou P, Appleton CC, Stensgaard AS, et al. Remote sensing, geographical information system and spatial analysis for schistosomiasis epidemiology and ecology in Africa: a review. Parasitology. 2009;136(13):1683–93.
doi:10.1017/S0031182009005998 - Clements ACA, Lwambo NJS, Blair L, Nyandindi U, Kaatano G, Kinung’hi S, et al. Bayesian spatial analysis and disease mapping: tools to enhance planning and implementation of a schistosomiasis control programme in Tanzania. Trop Med Int Health. 2006;11(4):490–503.
doi:10.1111/j.1365-3156.2006. 01594.x - Onyekachi Esther Nwoko, Tawanda Manyangadze et Moses John Chimbari dans leur article “Spatial distribution, abundance, and infection rates of human schistosome-transmitting snails and related physicochemical parameters in KwaZulu-Natal (KZN) province, South Africa”. PMC

