خصائص غذاء ملكة النحل (مراجعة علمية)
Properties of Royal Jelly: A Scientific Review
مها داود سلمان*1، أ.م مريم عبد الباري عريبي*2، أ. د. ضياء فالح الفكيكي*3
* قسم علوم الأغذية، كلية الزراعة، جامعة البصرة، العراق.
1 agripg.maha.salman@uobasrah.edu.iq
2 mariam.ouraiby@uobasrah.edu.iq https://orcid.org/0000-0001-7551-5699
3 dhia.alfekaiki@uobasrah.edu.iq https://orcid.org/0000-0002-7510-5881
DOI: https://doi.org/10.53796/hnsj67/39
المعرف العلمي العربي للأبحاث: https://arsri.org/10000/67/39
المجلد (6) العدد (7). الصفحات: 593 - 628
تاريخ الاستقبال: 2025-06-07 | تاريخ القبول: 2025-06-15 | تاريخ النشر: 2025-07-01
المستخلص: يُعد غذاء ملكة النحل (Royal Jelly) من المنتجات الحيوية التي تفرزها عاملات نحل العسل، ويتميز بخصائص غذائية وطبية فريدة تجعله ذا أهمية كبيرة في مجالات التغذية والصحة. يتكوّن هذا الغذاء الطبيعي بشكل أساسي من الماء (60-70%)، البروتينات (12-15%)، الكربوهيدرات (10-16%)، إضافة إلى الدهون (3-6%)، إلى جانب احتوائه على الفيتامينات والمعادن والأحماض الأمينية النادرة. تسلط هذه المراجعة الضوء على الخصائص الكيميائية والفيزيائية لغذاء ملكة النحل، وأبرز مكوناته الحيوية النشطة مثل حمض 10-HDA، إضافة إلى فوائده الصحية المتعددة التي تشمل التأثيرات المضادة للأكسدة، والمضادة للبكتيريا، والمنشطة للمناعة، فضلاً عن دوره في تحسين الأداء التناسلي والوظائف العصبية. كما تستعرض الدراسة أهم التطبيقات العلاجية لهذا الغذاء في الطب البديل، مع بيان العوامل المؤثرة على جودته وكفاءته، مثل نوع النحل، النظام الغذائي، وطرق الحفظ. وخلصت الدراسة إلى أن غذاء ملكة النحل يُعد مكملاً غذائيًا واعدًا يستحق مزيدًا من البحث لتحديد جرعاته المثلى وتأثيراته الفسيولوجية.
الكلمات المفتاحية: غذاء ملكة النحل، المركبات الحيوية، الفوائد الصحية، التركيب الكيميائي، الاستخدامات العلاجية.
Abstract: Royal jelly is a biological product secreted by worker honeybees and is characterized by unique nutritional and medicinal properties that make it highly valuable in the fields of nutrition and health. This natural substance mainly consists of water (60–70%), proteins (12–15%), carbohydrates (10–16%), and fats (3–6%), in addition to containing rare vitamins, minerals, and amino acids. This review highlights the chemical and physical properties of royal jelly and its most active bio-components, such as 10-HDA acid. It also explores its various health benefits, including antioxidant, antibacterial, and immune-boosting effects, as well as its role in enhancing reproductive performance and neurological functions. The study further outlines the therapeutic applications of royal jelly in alternative medicine and discusses the factors influencing its quality and efficacy, such as bee species, diet, and storage methods. The study concludes that royal jelly is a promising nutritional supplement that warrants further investigation to determine optimal dosages and physiological effects.
Keywords: Royal jelly, bioactive compounds, health benefits, chemical composition, therapeutic uses.
نبذة عن الغذاء الملكي Royal Jelly
غذاء ملكات النحل مادة شبه بيضاء لزجه تشبه الهلام وهي شكل من اشكال أفرازات الغـــدد البلعوميـــة والفك السفلي من النحل العامل ويعرف أيضا” باسم الطعام الخارق الذي تستهلكـه ملكة النحل فقط. يتـم تغذية يرقات نحل العسل بغذاء ملكات النحل عند الفقس وهو الغذاء الذي يتم تقديمه لليرقات الصغيرة فــــي أول (2-3) أيام مــــن النضج الى جانــب استخدامــه كغـــذاء مخصص لملكة النحل طوال فترة حياتهـــا بأكملها. Royalactin هـو المركب البروتيني الرئيسي في غـذاء ملكات النحــل الذي يسمـح بالتغيـرات المورفولوجية من حيث نمو الجسم وتطور المبيض لليرقة لتصبح ملكة النحل ويعد هذا الطعام الخارق هو السبــــب الرئيسي لطول عمر ملكة النحل مقارنة بالنحل الأخر. يحتوي الغذاء الملكي عدد كبير من المركبات النشطـــة بيولوجيــا ومن ضمنها decenoic acid2 10-Hydroxy- وهــو حامـض دهني غيـــر مشبــع. كما يعتبر الغذاء الملكي ذو فعاليـــة عالية فـــي الصحة الإنجابيـة من خلال تحفيز الهرمونات المسؤولة عــــن الخصوبـة وسن اليأس لدى النساء(2017Pasupuleti et al.,) .يعتبر غذاء ملكة النحل منتج طبيعـي مغذيًا وغنيًا بالبروتينات والأحماض الأمينية والفيتامينات المختلفة ويعتبـــر ذو محتــوى مائــي مرتفــع، حيـث يمثــل 60 – 70٪ مــن إجمالي تركيبتــه تليهــا الكربوهيـــدرات بنسبــة 11-23٪، والبروتينـات (9-18٪)، والدهــون (4-8٪)، والمعــادن (0.8-3٪)، والفيتامينات والفينــولات والأحمـاض الأمينيــة (Balkanska et al.,2012).
يعتمد تكوين غذاء ملكة النحل على العديد من العوامل ومنها الظروف الموسمية والإقليمية للتغذية والايض والتغيرات في فسيولوجيا النحل وعمر النحل وان انتاج غذاء ملكة النحل لكل مستعمــرة يتأثــر بالظــروف البيئيــة وخصائص مصــــــــــدر الرحيــــــــق ومحتوى المعـــادن والفيتامينــــــــــات فضلا” عــــــــــــــــن ظروف التخزيــــــــــــــن بعــــــد الحصاد (2016., Fratini et al) وقد استخدم هذا المنتــج مــن خلايــا النحـل فــي الطـــب التقليــدي والشعبــي لرعايــة صحــة الإنســان (El-Guendouz et al., 2020).
- التركيب الكيميائي Chemical composition
1-1- الرطوبة Moisture
تتأثر قدرة معالجة غذاء ملكات النحل ومدة صلاحيته وقابليته للاستخدام وجودته بمحتواه من الرطوبة لذلك فإن تقدير محتوى الرطوبة بدقة أمر ضروري لتحديد جودة غذاء ملكات النحل تتراوح نسبة الرطوبة في غذاء ملكات النحل الطازج ما بين 60 – 70% وقد تنخفض الرطوبة في غذاء ملكة النحل المجفف بالتجميد بنسبة 3.8% بسبب عملية التسامي والتجفيف. يتم داخل الخلية ضمان اتساق محتوى الرطوبة بشكل أساسي من خلال التزويد المستمر بإمدادات جديدة من عاملات النحل وخاصية امتصاص الرطوبة المتأصلة في غذاء ملكات النحل وجهود المستعمرة للحفاظ على مستوى الرطوبة المحيطة. فضلاً عن أن عدم قابلية بعض المركبات للذوبان يفسر الاختلافات في محتوى الماء (Sabatini et al., 2009). بين (2009)Szczesna et al. بعض التقنيات المعتمدة المختلفة لقياس كمية الرطوبة في غذاء ملكات النحل مثل التجفيف وطريقة كارل فيشر (Karl Fisher) والتجفيف بالتجميد (lyophilization). في هذا السياق هناك العديد من الطرق لتجفيف عينات غذاء ملكة النحل الخام بما في ذلك فرن التجفيف بالتجميد وفرن التفريغ والتجفيف بالأشعة تحت الحمراء (Almeida-Muradian et al., 2020 ) إذ تُعد طريقة كارل فيشر الكلاسيكية هي الأكثر شيوعا“ فهي أكثر دقة لأنها تعتمد على تفاعل كيميائي يتطلب وجود الماء وخصوصية شديدة لتحديد الماء دون الكشف عن مواد متطايرة أخرى ونطاق تحديد واسع من الرطوبة يتراوح بين 0.001٪- 100٪ . فضلاً عن كونها طريقة سريعة مع الحد الأدنى من تحضير العينة في حين أن التقنيات الأخرى تستغرق وقتًا طويلاً أو تتطلب معدات. أفادت العديد من الدراسات بوجود علاقة بين محتوى الرطوبة في غذاء الملكات الطازج وفترة الحصاد. تزداد نسبة الرطوبة بسرعة بين 24 و 48 ساعة بعد التطعيم ثم تدريجيا حتى 72 ساعة وتكون منخفضة للغاية في اليوم الرابع (Kanelis et al., 2015). درس Chen et al. (2015)المحتوى الرطوبي لنحل شينجيانغ الأسود الذي تنتمي الى نفــس سلالــةmellifera Apis والمعروفة أيضا باسم نحلة أيلي السوداء وهي واحدة من أربعة أنواع رئيسية من أنواع النحل في العالم وينتشر النحل الأسود في عدة مناطق من الصين وأماكن أخرى ويتغذى النحل الأسود على الزهور التي تنمو في الأماكن المرتفعة ويعتبر غذاء ملكة النحل احد منتجات النحل الأسود العامل ويحتوي على الكثير من المكونات الكيميائية ووجد بأنه يحتوي على الرطوبة بنسبة (60-70) % ويتأثر المحتوى الرطوبي والمكونات النشطة الأخرى في غذاء ملكة النحل بالعديد من العوامل مثل نوع النحل ومصادر العسل وموسم الإنتاج واختلافات المناخ ونمو النحل وتطوره. بين ( Kolayli et al. (2015في دراسة عن الخصائص الكيميائية ومضادات الأكسدة المختلفة لعينات غذاء ملكة النحل الأناضولي، وجد بأن قيم المحتوى الرطوبي للعينات المدروسة تراوحت بين (61.6- 73.0%) وكان متوسط القيم للمحتوى المائي (66.8%). تعتبر الرطوبة من العوامل التي تحدد جودة غذاء ملكات النحل لذلك يتم دراسة محتواه من هذه المكونات باستخدام الطرق الطيفية بواسطة التحليل الوزني وبين ( 9 Kazemi et al.,201) بأنه تم تحليل عينات من غذاء ملكة النحل الطبيعي ومقارنتها مع عينات غذاء ملكي مصنعة تجارياً واشار أن المكونات الكيميائية لغذاء ملكة النحل الطبيعي مشابهة لما وجده في غذاء ملكة النحل المصنع تجاريا“ ألا ان نسب المكونات تختلف فيما بينها حيث كانت نسبة الرطوبة في العينة المصنعة تجاريا“ اعلى من الطبيعية والماء هو عنصر مهم في غذاء ملكة النحل الطبيعي (Kausar & More, 2019) إذ يشكل نسبة عالية تبلغ 67% مما يسلط الضوء على خصائصه في مختلف مجالات الطب والصناعات الغذائية وغيرها Ajitha et al ., 2019)). بينت الدراسات من خلال تحليل العينات بأن نسبة الرطوبة في غذاء ملكة النحل هي (61.70-76.80 %) (Bazeyad et al.,2022). أشار (2024et al. ( Alkindi بأن المحتوى الرطوبي يعد من أهم المكونات الكيميائية في غذاء ملكة النحل المحلية وبنسبة كبيرة مقارنة بالمكونــات الأخرى. يختلف التركيب الظاهري لغذاء ملكة النحل باختلاف المواقع بسبب الظروف الخارجية ومصادر الرحيق ونوع النحل مما يؤثر على جودة وكمية غذاء ملكة النحل بالرغم من ثبات تركيبــه.
1-2- الرماد Ash
يعتبر الرماد من المكونات الأساسية في غذاء ملكة النحل حيث يمثل نسبة (0.8- 3 %) من المادة الطازجة منه في حين كانت النسبة في العينة المجمدة بالتجفيف (2-5% ) (Sabatini et al., 2009) وتم تثبيت هذه النسبة عالميا” ضمن المعايير الدولية والرماد هو المادة المتبقية بعد حرق المادة الغذائية حرقا“ تاما“ ويعتبر من المكونات الكيميائية الأساسية الموجــودة في غذاء ملكة النحل وبنسب مختلفة.
تم تحليل تركيبة غذاء ملكة النحل الطبيعي والمصنع تجاريا” وتبين بأن كلا العينتين تحتوى على نسبة رماد مختلفة( 9 (Kazemi et al., 201. كما وضح (and More,( 2019 Kausarعند دراستهم لعينة طازجة من غذاء ملكات النحل وعينة مجففة بالتجميد فقد كان محتوى الرماد في العينة الطازجة هو 1.22% بينمــا كانت في العينــة المجففة بالتجميـد 2.59%.
تركيبة غذاء ملكة النحل المحلية تحتوي على نسبة من الرماد تبلغ (1.06%) حيث تم استخراج المحتوى الكلي للرماد من خلال حرق كمية من غذاء ملكة النحل على درجة حرارة 600 مْ لمدة 4 ساعات وحساب الوزن المتبقي من المادة المحترقة وحساب محتوى الرماد الكلي من خلال المعادلة Ajitha et al.,2019)).
بين (and El-Kazafy,(2021 Al-Kahtani عنــد دراستهـــم لتأثير وقت جمع العينات على التركيب الكيميائي لغذاء ملكة النحل المحلية عند اختباره بعــد (24-48-72 ) ساعة بعـد الجمع وتبين بأن محتوى الرماد لكل العينات المحصودة خلال الثلاث مراحــل من الوقــت كان خـــلال 24 ساعة الأولى هو 1.96% بينما كان خلال 48 ساعة 2.47% وخلال 72 ساعة كان محتـوى الرماد 3.03%.
1-3- البروتينات Proteins
تعد البروتينات احد المكونات النشطة حيوياً والرئيسية في تركيب غذاء ملكة النحل وتعتبر العامل الرئيسي في تطور ملكة النحل ((Ramanathan et al.,2018 وأكد (Flanjak et al.,(2019 بأن غذاء ملكة النحل غني بالبروتينات وتتراوح نسبتها حوالي 11% وبين (Zhang et al.(2020 بأن غذاء ملكة النحل يحتوي نسبة من البروتينات التي تعد من المكونات الكيميائيـــة الأساسية فـــــــــــي غذاء ملكات النحل وبلغـــت نسبتــــه حـــــــوالي (12.5%).البروتينات الرئيسية في غذاء ملكات النحل (MRJPs) هي البروتينات التي تفرزها نحلة العسل، تتكون من تسعة بروتينات، وهي MRJP1 ويسمى أيضًا رويالاكتين ( (Royalcatin وMRJP2 وMRJP3 وMRJP4 وMRJP5 وهي موجودة في غذاء ملكات النحل الذي تفـــــــــرزه العاملات. MRJP1 هــــــــــو الأكثر وجــودًا والأكبــــر حجمــــــــا“ (Zhang et al., 2012 ). تشكل البروتينات الخمسة 82-90٪ من إجمالي البروتينات في غذاء ملكات النحل وهو غذاء غني بمزيج من المغذيات منها الفيتامينات والسكريات والدهون والبروتينات والإنزيمات أيضًا يحتوي على كميات عالية من الأحماض الأمينية اللازمة لتغذية كل من ملكة النحل واليرقات. الأرجينين، الهيستيدين، الأيزوليوسين، الليوسين، اللايسين، الميثيونين، فينيل الأنين، الثريونين، التربتوفان والفالين هي الأحماض الأمينية الأساسية العشرة الأكثر شيوعًا في MRJPs حيث يحتوي MRJP1 على 48% وMRJP2 على 47% وMRJP3 على 39.3% وMRJP4 على 44.5% وMRJP5 على 51.4% وMRJP6 على 42% وMRJP7 على 48.3% وMRJP8 على 49.5% وMRJP9 على 47.3 % من محتوى الأحماض الأمينية. يحتوي MRJP5 على نسبة عالية من الأرجينين والميثيونين بينما الأحماض الأمينية الموجودة في MRJP1 وMRJP2 وMRJP4 هي الليوسين والفالين. الأحماض الأمينية الرئيسية في MRJP3 هي الأرجينين والليسين. تعتبر البروتينات من المكونات النشطة لغذاء ملكات النحل حيث تتراوح نسبة البروتينات فيه (9-18%) وبروتينات غذاء ملكة النحل الرئيسية (MRJPs) تمثل أساس بنية غذاء الملكات حيث تشكل اكثر من 50% من وزن المادة الجافة منه وتم تحديد تسعة بروتينات مهمة في غذاء ملكة النحل ذات اوزان جزيئية مختلفة والتي تعتبر مسؤولة عن تطور اليرقات من خلال تزويدها ببعض الاحماض الامينية الأساسية حيــــــــــــث أن MRJPs1 هو بروتين سكــــــــــــــــري الرئيسي الموجود فـــي غذاء ملكة النحل RJالذي يكون وزنه الجزيئي (55) كيلو دالتون ويمتـــلك مجموعة واسعة من التأثيرات الصيدلانية على صحة الانسان مثــــل ألتئام الجروح ومضــادات الجراثيــم ومضادات الفطريات ونقص الكولسيترول ومضــاد للأورام وانشطة تعزيز الصحة وأيضأ يلعــــب دورا” في تحديد جودة غذاء ملكة النحل وحسب ظــروف التخزين (Bagameri et al., 2022)& Collazo et al.,2021)).
1-4- الدهون Lipids
وضــح (Balkanska and Kashamov,(2011 عنــد دراستهم للمكونات والخصائص الفيزيائية والكيميائية لغذاء ملكة النحل المجفف بالتجميد في بلغاريا بعد حفظ العينات بدرجة -18 مْ قبل التحليل حيث تبين بأن نسبة الدهون هي (3,09-8,56٪ ) من المحتوى الكلي. أن غذاء ملكة النحل المحلية يحتوي في تركيبته الكيميائية على نسبة (3.48-10.18%) من الدهون عند دراسته لخصائص مضادات الأكسدة لمنتج يحتــوي علـى بكتريا Lactobacillus acidophilus المضاف أليها 2.5% من غذاء ملكة النحل في الحليب الخالي الدهن وبكتيرياBifidobacterium bifidum المُضاف إليها 7.5% غذاء ملكات النحل في الحليب الخالي من الدسم (Nabas et al., 2014) .
أجرى (Ajitha et al. (2019 دراسة على غذاء ملكة النحل مـــن نحل العســــل الهنـــدي A.cerana حيث أظهرت التحليلات التي أجريت على غذاء ملكة النحل RJ وجود نسب من المكونات الكيميائية الحيوية التي تعزز وتدعم الصحة ومن بينها الدهون والتي وجدت بنسبة (3-8%) بينما كانت نسبة الدهن في العينة الجافة من غذاء ملكة النحل هي (8-19%) ويعتبر حامض ديسينويك-2-هيدروكسي-10 هو احد اهم الاحماض الدهنية فيه. غذاء ملكة النحل يحتوي على (3-6 %) دهون في تركيبه عند استخدام غذاء ملكة النحل في دراسة اجراها حيث استخدم غذاء ملكة النحل تقليل تلف الانسجة العضلية ( .(Asalan et al., 2021
تعتبر الدهون والليبيدات هي المكون الأساسي الذي يحافظ على التوازن الداخلي لجسم الانسان وتساهم في العمليات الحيوية للجســم والدهون هــي مركبات دهنية او شمعيـــة او زيتية قابلة للذوبان فــي المذيبــات العضوية ولا تذوب في المذيبـــات القطبيــة مثـــل المـــاء وتشمـــل الدهـــون على الزيــوت والدهون الثلاثيــة والفوسفوليبيدات والشمع والستيرويدات (Ahmed et al.,2023).
1-5-الكربوهيدرات Carbohydrates
ذكر) Sabatini,(2009 أن الكربوهيدرات تمثل حوالي 30% من المادة الجافة في غذاء ملكة النحل. تتكون بشكل أساسي من أحاديات الفركتوز والكلوكوز، التي تكون ثابتة نسبيًا وتوزيعها مشابه لتوزيع العسل. تمثل كمية الفركتوز والكلوكوز 90% من إجمالي السكريات الموجــــــودة في غذاء ملكة النحل مما يجعلهــا أكثر أنواع السكــر وفــرة فيـــه Xue et al., 2017)).
أظهرَ (Wytrychowski et al. (2013 أن تحديد السكريات يمكن أن يوفر معلومات مهمة حول جودة غذاء ملكة النحل بما في ذلك الكشف عن الغش المحتمل بالعسل أو السكريات المضافة وبين انه عند تغذية النحل على غذاء صناعي زادت محتويات المالتوز والمالتوريوز والسكروز والإيرلوز في غذاء ملكة النحل بنسبة تصل إلى 5.0٪ و 1.3٪ و 4.0٪ و 1.3٪ على التوالي بينما في العينات الأصلية يجب أن تكون هذه الكميات 0.2٪ غير قابلة للكشف 0.2٪ و 0.2٪ على التوالي.
أن محتوى الفركتوز والكلوكوز يتراوح بين 2.3-7.8٪ و3.4-7.7٪ على التوالي في عينات غذاء ملكة النحل الإيطالية والفرنسية، و 2.3-6.9٪ و3.7٪-8.2٪ على التوالي في عينات غذاء ملكة النحل من إيطاليا (روما) (Sesta,2006) كما يميل محتوى السكر إلى التغير على أساس متوسط مع التغييرات الغذائية حيث أظهرت العينات التي تم جمعها بعد إطعام بعض النحل شراب السكر وترك البعض الآخر يتغذى طبيعيا” وبعد الكشف عن محتوى السكريات لوحظ وجود اختلافات في تركيبته بين النحل المتغذي طبيعيا“ والنحل المتغذي صناعيا“ بالسكريات الصناعية وبالتالي، يمكن أن يساعد البحث في محتوى السكر الى التمييز بين غذاء ملكات النحل المصنوع باستخدام تقنيات مختلفة، وتحديد طريقة التصنيع، والعمل كوسيلة تكميلية للكشف عن غذاء ملكات النحل التجاري غير المحدد (Daniele and Casabiana, 2012).
بين (Balkanska,(2018 بأن نسبة الكربوهيدرات في غذاء ملكة النحل تتراوح بين (10–15%) ويشكل الكلوكوز والفركتوز أكثر من 90% من إجمالي محتوى السكر في غذاء ملكات النحل ومن بين السكريات الأخرى التي تم الإبلاغ عنها بكميات ضئيلة السكروز والمالتوز والتريهالوز والمليبيوز والريبوز والإيرلوز ويختلف محتوى السكر بناءً على أصل غذاء ملكات النحل ومصدره النباتي ولكن بشكل عام لا تختلف النسب المتوسطة للفركتوز والكلوكوز بشكل كبير بين العينات من مناطق مختلفة.
تعتبر السكريات جزءًا مهمًا من تقييم جودة غذاء ملكات النحل وقد أثبتت الأبحاث أن سكريات غذاء ملكات النحل تتكون بشكل أساسي من الفركتوز والكلوكوز والسكروز وتشكل حوالي 7-18% من العينات الطازجة في غذاء ملكات النحل المجفف بالتجميد ويتم تحطيم تركيب الكربوهيدرات عن طريق التجفيف بالتجميد لتصل إلى 1.28% ((Kausar & More, 2019. طور Zhu et al. (2019) طريقة فصل IC-PAD كروماتوغرافيا الأيونات مع الكشف الأمبيروميتري النبضي ذات الحساسية العالية وقابلية الإنتاج لتوصيف وتحديد كمية 19 نوعًا من السكر في عينات غذاء ملكات النحل وقد تم تطبيق الطريقة على 100 عينة مختلفة من غذاء ملكات النحل من ثلاث مقاطعات وقد تم الإبلاغ عن الحد الأقصى والأدنى والمتوسط لمحتوى السكريات بالإضافة إلى الانحراف المعياري ومعامل التباين وقيم التماثل لجميع عينات غذاء ملكات النحل ولم يتم الكشف عن الكالاكتوز والرايبوز في أي من عينات غذاء ملكات النحل.
1-6- الفيتامينات Vitamins
تُعتبر الفيتامينات مواد أساسية ضرورية لصحة الجسم ونموه الطبيعي، ويجب أن يحصل الجسم على كميات كافية منها عبر الغذاء و في حال عدم كفاية هذا المدخول أو وجود احتياجات غذائية خاصة يُنصح بتناول مكملات متعددة الفيتامينات للوقاية من نقص الفيتامينات( Rehman et al.,2008)
وضح and De Almeida-Muradian,(2009) Moreschiمن خلال الدراسات التي أجريت على عينات غذاء ملكة النحل من مدينة ساو باولو في البرازيل وجد بأنه يحتوي على أربعة فيتامينات من مجموعة B وبين بأن غذاء ملكات النحل ليس مصدرًا مهمًا للفيتامينات التي تم تحليلها على الرغم من أن النتائج تشير إلى أن التقنية المستخدمة مناسبة لتحديد هذه الفيتامينات الأربعة ومركباتها. الفيتامينات القابلة للذوبان في الماء B1 و B2 و B6 و PP هي مواد عضوية أساسية للكائن البشري، تعمل كإنزيمات مساعدة في العديد من العمليات الأيضية. حددت الفيتامينات بواسطة تقنيةHPLC باستخدام عمود C18. تم تحليل أربع عينات من مصدرين مختلفين، وتراوحت النتائج من 0.08 إلى 0.41 مجم / 100 جم (فيتامين B1 أو الثيامين)؛ من 0.01 إلى 0.05 مجم / 100 جم (فيتامين B2 أو الريبوفلافين)؛ من 0.13 إلى 0.38 مجم / 100 جم (بيريدوكسال – فيتامين B6)؛ من 0.26 إلى 1.38 مجم / 100 جم (بيريدوكسامين – فيتامين 6B)؛ من 0.21 إلى 0.57 ملغ/100 جرام (نياسين – فيتامينPP)؛ ومن 1.56 إلى 2.00 ملغ/100 جرام (نياسيناميد – فيتامينPP).
ذكر (2016),Yuksel and Akyol من خلال الأبحاث التي أجريت على منتجات النجل خصوصا” غذاء ملكة النحل بأنه مصدر جيــد للفيتامينات ( B2,PP,B1) .
وجد (Xue et al., (2017b عند دراسة تركيب غذاء ملكة النحل ومن ضمنها الفيتامينات حيث بين بأنه لا توجد سوى كميات ضئيلة من فيتامين C .
اشار (Collazo et al.,2021) بأنه من خلال تحليل نماذج عينات غذاء ملكة النحل توصل الباحثون الى تركيبته ومحتواه من الفيتامينات حيث يعتبر مصدر جيد لفيتامين B1 بالإضافة الى نسبة قليلة من فيتامين E.
2- العناصر المعدنية: Mineral elements
أن الاختلاف في محتوى العناصر المعدنية في منتجات النحل له تأُير واضح في تغير لون العسل وغذاء ملكة النحل وبحسب المصدر الزهري حيث كلما ازدادت نسبة العناصر المعدنية يميل منتجات النحل الى اللون الغامق ولهذا السبب حددت Codex لعام 2001 محتوى العناصر المعدنية في العسل والمنتجات الأخرى للنحل بحيث يجــــب ان لا يزيـــــد محتوى المعادن عــــــــن 0.6 % فـــــــي العســـل الطبيعي (Cornelia and chis, 2011 ).
ذكر Nayik and Nanda,(2015) في دراستهما على اصناف العسل الهندي إن معدل نسب العناصر المعدنية تراوح بين 0.05 – 0.06 % في حين إن معدل نسب العناصر المعدنية في اصناف من العسل البنغلاديشي هو 0.03 % ولوحظ تفوق نسب الصوديوم والبوتاسيوم والكالسيوم مقارنة مع المعادن الأخرى.
بين ( Asaduzzaman et al. (2015بأن الاختلاف في نسب العناصر المعدنية يعود للمنطقة الجغرافية ومصدر النبات و تأثيره على تركيز نسب الرماد في العسل ومنتجات النحل.
عند تحليل غذاء ملكة النحل فيزيائيا” وكيميائيا تم قياس تركيز المعادن باستخدام مطيافية الامتصاص الذري باللهب حيث أكد بأنه يحتوي على المعادن بتراكيز محددة ووجد بأن البوتاسيوم والمغيسيوم والصوديوم والكالسيوم تتواجد في غذاء ملكة النحل بأعلى التراكيز et al.,2016) MUREŞAN ).
ان محتوى العناصر المعدنية يتأثر بالتنوع النباتي الرحيقي تأثرا كبيرا إضافة الظروف البيئية والأساليب المتبعة في إدارة المناحل وطريقة جمع منتجات النحل . كما تتفاوت نسب ومحتوى العناصر المعدنية في منتجات النحل بفعل الاختلافات في اصل الازهار حيث يلعب محتوى المعادن دورا حيوي في تحديد لون العسل وغذاء ملكة النحل ومنتجات النحل الأخرى وقيمتهم الغذائية .(Mulugeta et al., 2017)
يمثل المغنيسيوم النسبة الأعلى من العناصر المعدنية الموجودة في غذاء ملكة النحل إضافة” الى الزنك والحديد وهذا ماأكدته الأبحاث التي درست تركيب غذاء ملكة النحل والكشف عن العناصر المعدنية فيه (et al.,2017 Balkanska).
أشار Saeed and Jayashankar,(2020) ان محتوى العناصر المعدنية يتأثر بالتنوع النباتي ومصدر الرحيق تأثرا كبيرا إضافة“ الى الظروف البيئية والأساليب المتبعة في إدارة المناحل وطريقة جمع منتجات النحل.
يحتوي غذاء ملكة النحل في تركيبته الغنية بالمكونات النشطة على العناصر المعدنية حيث انه عند دراسة التركيب الكيميائي للغذاء الملكي الذي تم حصاده من النحل العامل والمتغذي على فطائر حبوب لقاح البلـوط وبذور اللفت لبيان تأثير نسبة العلف على مكونات غذاء ملكة النحل وبينت النتائج بأن العناصر المعدنية موجودة بوفرة فيه Ghosh and Jung,2024)).
3- الرقم الهيدروجيني pH
الأس الهيدروجيني هو مقياس لوغارتيمي يمثل تركيز ايونات الهيدروجين ( +H ) في منتجات نحل العسل حيث إن تقديره مفيد كمتغير مساعد لمعرفة جودة المنتج وكمعامل لتقييم الحموضة الكلية يعزى أنخفاض قيم pH أساسا” الى وجود حامض الكلوكونيك Gluconic acid الذي يتكون بفعل أكسدة سكر الكلوكوز وله دور اساسي في ثبات منتجات النحل ضد التلف بالأحياء المجهرية (Bogdanov, 2009). نظرًا لاختلاف درجاتها الهيدروجينية خلال دورة حياتها تُصنع البروتينات في الغدد البلعومية السفلية للنحل المرضع كبروتينات افرازية وتترجم مباشرة الى الشبكة الاندبلازمية للخلايا الافرازية عند درجة حموضة تبلغ حوالي 7.02 بعد ذلك تخزن البروتينات في حويصلات عند درجة حموضة تتراوح بين (5.5- 5.1 ) وبعد افرازها من الغدد البلعومية السفلية تتعرض البروتينات الى افرازات الغدد الفكية السفلية الحامضية عند درجة حموضة (0.1-3.9) المكونة من الاحماض الدهنية مما يؤدي الى درجة حموضة نهائية تبلغ (4.0) في غذاء ملكة النحل إضافة الى منتجات النحل الأخرى ومنها العسل الذي تبلغ درجة الحموضة فيه (4.5 – 5.2) (Mandacaru et al.,2017)& Helbing et al.,2017)). لكي تؤدي البروتينات وظائفها الحيوية يجب ان تكون درجة الحموضة مستقرة وضمن النطاق (4.0- 7.0) وتختلف البروتينات بعضها عن بعض بدرجة استقرارها عند الاس الهيدروجيني فبعضها يستقر عند درجة حموضة (7.0-7.5) بينما البعض الأخرى تكون درجة استقراره (4.5) درجة حموضة . وتصل اعلى نسبة للرقم الهيدروجيني في غذاء ملكات النحل عند درجة (4.0).
كما وضح ( Flannjak et al. (2019بأنه تم تحديد الخصائص الفيزيائية والكيميائية من حيث الرطوبة ومحتوى البروتين وقيمة الرقــم الهيدروجينــي والحموضة الكلية وتركيـــب الكربوهيــــدرات ومحتــوى 10-HDA في العديد من البلدان بأستثناء كرواتيا وتدوين المعلومات في قاعدة بيانات خاصة لكل بلد وبسبب استخدام غذاء ملكة النحل في التغذية البشرية او كمكون حيوي نشط مع مواد ومنتجات أخـــــرى ( مكملات غذائية او دوائية) تم تحليل غذاء ملكة النحل في ثلاثة عشر عينة غذاء ملكي كرواتي بهدف فهم جودة غذاء ملكات النحل المنتج في كرواتيا حيث كانت النتائج التي تم الوصول لها مشابهة للمعيار الدولي ومن ضمنها الرقم الهيدروجيني حيث وجدوا أن قيم PH تراوحت بين ( 3.98- 4.21 ).
درس (Ajitha et al. (2019 المكونات الكميائية لغذاء ملكة النحل كونه منتج طبيعي يلعب دورا“ مهما في تحديد سلالة النحل وتطور ملكة النحل حيث لوحظ من خلال النتائج بأن الغذاء الملكي الذي تم جمعه من نحل العسل الهندي(A. cerana) أظهر درجة حموضة بمقدار 3.6. يلعب الرقم الهيدروجيني دورا“ مهما بالنسبة لبروتينات غذاء ملكة النحل الأساسية (MRJP) Major Royal Jelly Protiens وبما ان البروتينات تشكل نسبة (11-18%) من المكونات الأساسية في غذاء ملكة النحل والتي تضم عشرة بروتينات مختلفة (2019 ,Buttstedtand Mureşan( .
4- المجاميع الفعالة في غذاء ملكة النحل Active groups in Royal Jelly
4-1 الفينولات والفلافونيدات: Phenols and flavonoids
غذاء ملكة النحل (RJ) هو عنصر غذائي وظيفي مهم ويتملك العديد من الخصائص المعززة للصحة وقد اثبت بأن له العديد من الخصائص الوظيفية مثل النشاط المضاد للبكتريا والنشاط المضاد للألتهابات وانشطة توسع الاوعية الدموية وخفض ضغط الدم وله أيضا دور في تطهير الجروح ونشاطه العالي كمضاد للأكسدة وأيضا نشاطه المضاد للاورام وفرط كوليسترول الدم وتعزى هذا الفعالية العالية لمركب غذاء ملكة النحل بشكل أساسي الى الاحماض الدهنية الحيوية والبروتينات والمركبات الفينولية وتختلف هذه المكونات باختلاف الظروف الموسمية والأقليمية (Ramadan and Al-Ghamdi,2012). تشمل الفلافونويدات الفئات الأربع التالية: الفلافونونات (هسبريتين، نارينجينين، وإيزوساكورانيتين) والفلافونات (كريسين، أكاسيتين، ولوتيولين، أبيجينين، وجليكوسيده) والفلافونولات (جليكوسيدات كيمبفيرول وإيزورهامنيتين) والإيزوفلافونويدات (كوميسترول، جينيستين، وفورمونونيتين (Negro et al.,2014) . اجرى Ahmed et al.(2016) دراسة تضمنت فحص 16 عينة من عينات العسل الباكستاني جمعت من مناطق مختلفة لمعرفة إمكاناتها الفيزيائية والكيميائية وأيضا دراسة محتواها من الفينولات والفلافونيدات حيث كان اجمالي المحتوى الكلي للفلافونيدات بين 11.38 الى 57.66 ملغم / كغم. درس (Bakchiche.(2017 اجمالي محتوى الفينول والفلافونيدات ومضادات الاكسدة في العسل والبروبليس التي جمعت من منطقة الاغواط (جنوب الجزائر) حيث تم تحديد المحتوى الفينولي الكلي باستخدام كاشف فولن Folin-Ciocalteu reagent واستخدم حامض الكاليك كمادة قياسية بينما تم تحديد محتوى الفلافونويد حيث تم استخدام طريقة AlCl3 (تحليل كلوريد الألومنيوم ) مع حامض الرتين كمادة قياسية حيث أظهرت النتائج أن كمية المركبات الفينولية في عينات العسل كانت منخفضة (بين 38 و86 ملغم لكل 100 غم من العينة) بينما كانت مرتفعة بشكل ملحوظ في البروبوليس (2385 ملغم لكل 100 غم من العينة) وقد أظهرت الدراسة وجود علاقة إيجابية قوية بين محتوى الفينولات والفلافونويد ومضادات الأكسدة مما يشير إلى أن التركيزات العالية منها تعتبر مؤشراً جيداً على فعالية مضادات الأكسدة.
تعتبر منتجات النحـل مثــل العسـل وغذاء ملكة النحل والبروبولـيس وحبوب اللقاح والشمع مــن المنتجات الضروريــة التــي تفيــد البشر بسبـب المركبــات الفعالة النشطة بيولوجيا” الموجودة فيها والتي تشمل الفينولات والسكريـات والفلافونيدات وغيرها وتعــزى قابلية غذاء ملكة النحل وتأثيراتــه الواسعة في كونه مضاد للفيروسات وتعديل المناعـة ومضـاد للالتهاب ومضــاد للأورام السرطانية وتنظيم السكـر وضغط الدم ومضاد للشيخوخة والزهايمر وغيرها من الأنشطة البايلوجية الى وجود هـــذه المجاميـــع الفعالـة كمـــا يحتــوي غذاء ملكة النحل على الفينـولات النباتيـة التـي تعمـل كمضاد للأكسـدة بالإضافة الى الفـلافونيدات المضـادة لتصلـب الشراييــن وسكــر الدم لذلك يعتبــر غذاء ملكة النحل مــن المنتجات الضروريــة للصحــة بسبـب تأثيراتــه العلاجية ( Cornara et al.,2017).
غذاء ملكات النحل معروف منذ قرون طويلة لكنه شهد في الآونة الأخيرة زيادة ملحوظة في استهلاكه يعود ذلك إلى احتوائه على مركبات نشطة بيولوجيًا مثل الأستيل كولين، الببتيدات، هرمونات التستوستيرون، البروجسترون، البرولاكتين، الإستراديول، حمض الهيدروكسي ديكانويك (HAD)، أوكسيد الأدينوسين أحادي الفوسفات (AMP N1-) بالإضافة إلى البوليفينول والفلافونويد والأدينوسين وبفضل هذه المركبات يمكن اعتبار غذاء ملكات النحل غذاءً وظيفيًا ومغذيًا (Maghsoudlou et al., 2019).
بين Yelin and Kuntadi,(2019) بأنه تم دراسة المحتوى الكيميائي والمركبات النشطة للعسل من سلالة مشابهة لسلالة غذاء ملكات النحل (Apis mellifera ) وسلالة أخرى أيضا“من منطقتي جاوة وسومباوا حيث أجريت الفحوصات النوعية للكشف عن وجود المركبات (القلويدات، الفلافونيدات ، التانينات، الصابونين) وغيرها من المركبات ووجد بأنه جميع العينات من السلالتين تحتوي على الصابونين والفلافونيدات لكنها لاتحتوي على التانينات والقلويدات .
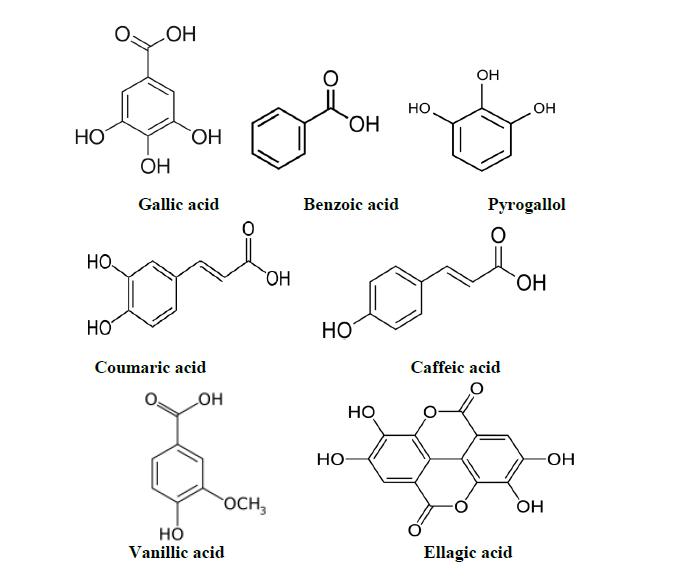
شكل(1) الصيغة التركيبة لبعض الحوامض الفينولية (Tsao,2010)
درس (Takruri and Alkhedr,( 2021 المحتوى الفينولي الكلي والقدرة المضادة للاكسدة ونشاط إزالة الجذور الحرة في غذاء ملكات النحل والعسل متعدد الازهار وعسل الحمضيات حيث تم تحليل العينات لمعرفة محتواها الفينولي الكلي باستخدام طريقة كاشف فولن حيث أظهرت النتائج ان المحتوى الفينولي في غذاء ملكة النحل اعلى من العسل متعدد الازهار وعسل الحمضيات حيث كانت نسبة الفينولات في غذاء ملكة النحل (9.30-621.60 ملغم /100 غم) بينما في العسل متعدد الازهار (1.13-16.92 ملغم /100 غم) وفي عسل الحمضيات (0.44-12.45ملغم /100 غم) أضافة“ الى قدرة عالية مضادة للأكسدة، وبما أن غذاء ملكة النحل غني بالمواد الفعالة النشطة لذلك عند تعرضه للضوء او الحرارة او الاوكسجين سوف يؤدي الى الحد من فعاليته (Sousa et al.,2025) .
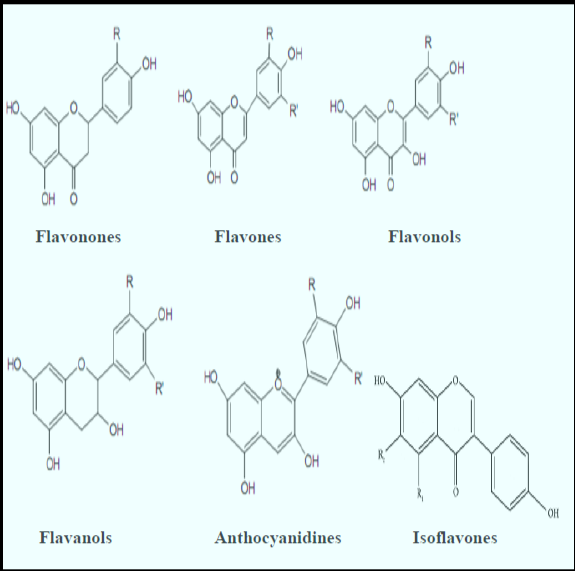
شكل (2)الصيغة التركيبية لبعض أنواع الفلافونيدات (Bahorun et al.,2006)
يلعب غذاء ملكة النحل دورا“ بيولوجيا“ في علاج العديد من الامراض وذلك بسبب المركبات الفعالة النشطة في هذا الغذاء الوظيفي ومن ضمنها الفينولات والفلافونيدات التي تلخص الدور الفعال لغذاء ملكة النحل في الحفاظ على صحة الانسان وتنظيم المناعة وأطالة العمر وغيرها ويحتوي على (1.28 ميكروغرام/ملغ) من الفلافونيدات الكلية و(23.3 ميكروغرام/غرام) من الفينولات) حيث تظهر المركبات الفينولية نشاطا“ مضادا“ للأكسدة والبكتريا (Guo et al,.2021). درس Altun and Aydemir,(2022) اجمالي محتويات الفينولات والفلافونيدات في مخاليط غذاء ملكات النحل حيث استخدم طريقة Folin-Ciocalteu حيث تراوحت قيمة TPC بين 0.6 و38.2 ملغ/ 100 غرام، وبلغ متوسط القيمة 11.08 ملغ/ 100 غرام ، في حين درس اجمالي محتويات الفلافونيدات باستخدام طريقة قياس اللون باستخدام كلوريد الألومنيوم حيث كان اجمالي قيم تركيز الفلافونيدات TFC بين 0.1 و 30.06 ملغم/ 100 غرام، بمتوسط قيمة 9.2 ملغم/ 100 غرام.
4- التانينات Tanins
تُعتبر التانينات من البوليفينولات التي تتشكل كمستقلبات ثانوية في النباتات، وقد شهد إنتاجها زيادة ملحوظة في الآونة الأخيرة نتيجة لاستخداماتها التجارية في مجالات الصناعات الغذائية والدوائية ومستحضرات التجميل (Capparucci et al., 2011). وقد أظهرت الدراسات أن للتانينات تأثيرات مضادة للأكسدة ومضادة للالتهابات (Faker El-Din et al., 2015). تشير معظم الأبحاث إلى أن كفاءة استخلاص التانينات من المصادر النباتية أو الحيوانية تعتمد على نوع المذيب المستخدم.
تُستخدم طرق متنوعة لاستخلاص المركبات الفعالة من المواد النباتية والحيوانية، وتنقسم هذه الطرق إلى قسمين: الطرق المتقطعة والطرق المستمرة، تشمل الطرق الرئيسية للاستخلاص المتقطع النقع، الغلي، الاستخلاص الكحولي، التخمير، الاستخلاص بالمذيبات، الاستخلاص بالموجات الدقيقة، والاستخلاص باستخدام السوائل فوق الحرجة، وغيرها أما بالنسبة للطرق المستمرة فإن أكثرها شيوعًا هي الاستخلاص بالمذيبات العضوية، الترشيح المستمر، الاستخلاص بالسوكسليت، والاستخلاص بتيار معاكس (Cobzaru, 2014). تختلف طرق الاستخلاص في العديد من الخصائص، بما في ذلك نوع المذيب ومبدأ الاستخلاص. بين Yelin and Kuntadi.(2019) عند دراسة المركبات الفعالة في سلالتين من العسل وبالأخص سلالة مشابهة لسلالة غذاء ملكات النحل (Apis mellifera ) منطقتي جاوة وسومباوا حيث بينت النتائج عدم وجود التانينات في العينات المدروسة.
اشار (2020) Oriolowo et al.في دراسة أجريت على عينات من العسل الذي تم جمعه من أربع ولايات في شمال ووسط نيجيريا لتحديد وجود المركبات النشطة ومن ضمنها التانينات حيث أظهرت النتائج وجود التانينات في العينات الأربعة جميعها وبين أن الموقع الجغرافي والبيئة يؤثران بشكل كبير على تركيب المركبات الفعالة وتراكيزها في العسل وكانت تراكيز التانينات في العينات الأربعة المدروسة هي (3.83-390.32 ملغم/100غم)(11.43-426.14 ملغم/100غم) (19.75-329.49 ملغم/100غم)(0.27-278.48 ملغم/100غم).
بين (2020). Umami et al بأنه من خلال الدراسات والتحاليل لغذاء ملكة النحل باستخدام طريقة تحويل فورييه للأشعة تحت الحمراء بالإضافة إلى استخدام الاختبارات الكيميائية النباتية لتقييم المكونات الموجودة في غذاء ملكات النحل تبين من خلال نتائج الفحوصات النوعية وجود التانينات حيث أعطت النتيجة موجبة بينما عند استخدام طريقة FTIR تم قياس كمية التانينات الموجودة في غذاء ملكة النحل وهي (0.09052 ملغم/مل) وبنسبة مئوية 0.95%. وضح (Mohiuddin et al. (2022 عند دراسته لمركب البروبوليس الذي هو احد منتجات نحل العسل وتحليل تركيبه الكيميائي من منطقة كشمير ووجد بأنه يحتوي على جزيئات نشطة بيولوجيا“ ذات وظائف واسعة حيث لوحظ بأنه محتواه غني بالمجاميع الفعالة كالقلويدات والصابونين والتانينات وغيرها.
5– النشاط المضاد للأكسدة في غذاء ملكة النحل Antioxidant activity of royal jelly
مضادات الاكسدةAntioxidants تعرف بأنها المركبات التي لها القدرة على إيقاف سلسلة من التفاعلات التي تنتج بسبب الجذور الحرة حيث تعمل على إعطاء الكترون الى الجذور الحرة وتتأكسد لحماية خلايا الجسم وتمنع تلفها حيث تنتج جذور ضعيفــــة غير فعالة وتساهـــــم في حماية الجسم (Fattouch et al.,2007) .شهدت الآونة الأخيرة اهتماما” واسعا بدراسة مكونات منتجات النحل مثل العسل وغذاء ملكة النحل وغيرها لكونها تمتلك خصائص متعددة حيث تمتلك المكونات الكيميائية للغذاء الملكي تأثيرا واضحا في تعزيز الصحة من خلال عملها كمضادات أكسدة طبيعية ومثبطات ميكروبية ومضادات للأورام والتقليل من خطر الإصابة بأمراض القلب والاوعية الدموية وتقوية المناعة ومضاد للالتهابات إضافة الى منع الامراض الوبائية والسرطانية كذلك تعمل مضادات الاكسدة على تأخير تلف الأغذية كالتزنح التأكسدي او تغير اللون الناتج عن الاكسدة بفعل الضوء والحرارة والمعادن اذ تعمل كمواد حافظة ( (Dimitrova et al.,2007.
وتعرف الأكسدة Oxydation هي عملية الاكسدة الحيوية التي تتم في النظام الحيوي لأنتاج الطاقة من خلال إضافة الاوكسجين او انتزاع الهيدروجين او انتزاع الالكترونات وينتج عنها الجذور الحرة Free radical التي تعرف بأنها مركبات كيميائية ( ذرات او جزيئات) تحتوي على الكترون واحد غير مزدوج وتسبب عدم استقرارها وتكون شديدة التفاعل, تقترن الجذور الحرة مع جزيئات بيولوجية مثل الدهون والبروتينات والاحماض النووية والكربوهيدرات من اجل استقرارها أذ لها القدرة على توليد جذور حرة أخرى تسبب احداث اضرارا للخلايا المحيطة وتكون سبب في حدوث بعض الامراض الخطيرة (Nagmoti et al., 2012).
أشارت العديد من الدراسات الى أن الأكسدة تتسبب في بعض الامراض مثل الشيخوخة وتلف الخلايا الحيوية اضافة الى العديد من المشاكل الصحية بفعل الجذور الحرة كنواتج ثانوية لأيض الاوكسجين تحتوي العديد من الأغذية على مضادات اكسدة تعمل بشكل جيد على كبح الجذور الحرة جزئيا او كليا” وبالنتيجة تؤخر الكثير من الامراض المزمنة((Alzahrani et al., 2012.
5-1- قابلية اقتناص الجذر الحر Free radical scavenging ability DPPH
يعتمد هذا الاختبار على قياس قابلية او قدرة مضادات الاكسدة على اقتناص الجذر الحر حيث يتم اختزال الالكترون المنفرد لذرة النيتروجين في DPPH (2,2-diphenyl-1picrylhydrazyl) عند طريق استقبال ذرة الهيدروجين من مضادات الاكسدة ويتحول الى الهيدرازين المقابل بعدها يحدث التفاعل اللوني للجذر DPPH ذو اللون البنفسجي الذي يتحول الى جزئية مستقرة DPPH-H وهي مادة صلبة ذو لون اصفر ويستعمل هذا الاختبار في تقييم نشاط المركبات التي تعمل كمضادات اكسدة ( .(Bahar et al.,2013
تعتبر منتجات النحل كالعسل وغذاء ملكة النحل من الأطعمة الوظيفية التي تحتوي على مركبات فينولية لها القدرة على التخلص من الجذور الحرة وبالتالي حماية الخلايا والانسجة الحية من الاجهاد التأكسدي المركبات الفينولية هي المكونات الرئيسية التي توفر الخصائص الوظيفية للأطعمة مثل القدرة المضادة للأكسدة( Uthurry et al.,2011 & Martos et al .,2008).
بين ( Liu et al .,2008) ان غذاء ملكة النحل الذي تم جمعه بعد 24 ساعة من نقل اليرقات لديه اعلى قدرة مضادة للأكسدة لان تأخير الحصاد يقلل من خصائص مضادات الاكسدة للغذاء الملكي لـذا القـدرة المضـادة للأكسدة للغذاء الملكي تقل مع طول فترة الخزن والحصاد إضافة الى تأثير عوامل كثيرة على جودة غذاء ملكة النحل منها نوع النبات ومصدر الازهار والمناخ والتربة والعوامل الوراثية والبيئية.
وضح (Lee.et.al.,2013&Serem.and.Bestsr,2012) عند دراستهم العلاقة بين الفعالية المضادة للأكسدة وبين تنوع المصادر الزهرية والاختلاف والمنطقة الجغرافية وطريقة جمع غذاء ملكة النحل والعسل وظروف التخزين تبين ان هناك ارتباطا” وثيقا بين الفعالية المضادة للأكسدة وبين التنوع في هذه العوامل. هناك علاقة وثيقة بين الفترات الخزنية لمنتجات النحل كالعسل وغذاء ملكة النحل وغيرها مع تغير نسب الفينولات اثناء الخزن.
وضح Khalil.et al.(2012c) عند دراستهم القدرة المضادة للأكسدة خلال الخزن لمدة سنة على عينات من عسل التيولنغ المعرضة الى اشعة كاما حيث بلغت الفعالية المضادة للأكسدة خلال الشهور الثلاثة الأولى 67.09% وبعد مرور فترة خزنية أخرى لمدة ستة اشهر انخفضت الفعالية المضادة للأكسدة تدريجيا حتى بلغت 65.26% واستمرت بالانخفاض حتى وصلت الى 44.65% عند مرور سنة كاملة ويرجع هذا الانخفاض الى تغيير نسبة الفينولات وقلتها تدريجيا اثناء الفترة الخزنية لذلك انخفضت معها تلقائيا” القدرة المضادة للأكسدة.
درس (Takruri and Alkhedr,(2021 الفعالية المضادة للأكسدة على غذاء ملكة النحل والعسل حيث توصلوا الى ان القوة المضادة للأكسدة ومحتوى الفينولات الكلي في غذاء ملكة النحل اعلى منها في العسل لان غذاء ملكة النحل تميز بمحتواه العالي من الفينولات الكلية والقدرة المانعة للأكسدة وأيضا“ بينوا ان هناك علاقة إيجابية بين المحتوى الكلي للفينولات وكل من قوة منع التأكسد والقوة الكابحة للجذور الحرة في غذاء ملكة النحل ونوعين من العسل المدروس وكانت القدرة المضادة للتأكسد باستخدام ( DPPH) لكل من غذاء ملكة النحل والعسل تزداد مع زيادة التركيز حيث بلغت القوة المضادة للتأكســد في غذاء ملكة النحل عنــد تركيــز mg/ml)50)هــي 35.5 % بينما ازدادت القوة المضادة للأكسدة بزيادة التراكيز تدريجيـا” الى أن بلغـت ( 79.30) عند التركيز mg/ml)500) كذلك نوعي العسل ازدادت القوة المضادة للأكسدة بزيادة التراكـيز حيث بلغت عنـــد تركيــز 50 mg/ml (14.07%) و(15.25%) لكلا النوعين وازدادت تدريجيا“ عند زيادة التراكيز حتى بلغت القوة المضادة للتأكسد عند التركيز (500 mg/ml) هي (47.46%) و(45.07%) على التوالي لكلا النوعين.
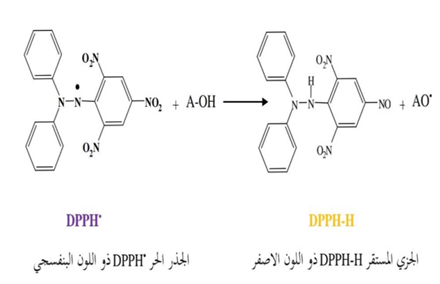
الشكل (3 )اقتناص الجذر DPPH بوجود عامل مضاد للأكسدة (آسيا, 2018)
5-2- القوة الاختزالية Redusing power
درس(2014).Nabas et al التأثير التآزري لغذاء ملكة النحل المضاف الى نوعين من البكتريا الحيوية وبنسب (2.5% ،7.5% ) حيث أظهرت النتائج بأن غذاء ملكة النحل يمتلك نشاطا“ مضادا” للأكسدة وقدرة اختزال عالية عند تركيز 1000 مايكروغرام/ مل حيث بلغت نسب تثبيط البيروكسيد للنوعين ( 52% ،42% ) على التوالي.
وضح Vulic et al. (2015) عند دراستهم لعسل النحل الصربي المأخوذ من مصادر زهرية متعددة بأن الفعالية المضادة للأكسدة تنخفض مع طول فترة الخزن حيث لوحظ بأن قيم القوة الاختزالية انخفضت عند مرور فترات زمنية . بين ( Bakchiche et al. (2017 في إطار دراسة النشاط المضاد للأكسدة من خلال اختبار القوة الاختزالية لبعض منتجات النحل (مثل العسل والعكبر) في ثلاث مناطق من جنوب الجزائر، أظهرت النتائج أن القوة الاختزالية بلغت 32% و0.0015% على التوالي، بينما سجلت عينات المقارنة 80% و62% لكل من حامض الأسكوربيك وBHT على التوالي.
وأشارت الدراسة إلى أن المحتوى الكلي للفينولات بالإضافة إلى المحتوى البروتيني يعتبران مؤشرين جيدين على فعالية مضادات الأكسدة في العكبر والعسل. تعتبر منتجات النحل مثل العسل وغذاء ملكة النحل وحبوب اللقاح والبروبليس وغيرها مصدرا مهما لمضادات الاكسدة الطبيعية القادرة على مواجهة آثار الاجهاد التأكسدي المتسبب في العديد من الامراض وتمتاز المركبات ذات الطابع الفينولي بكونها مواد قادرة على التخلص من الجذور الحرة وتعزى قدرة منتجات النحل على مقاومة الاكسدة الى محتواها العالي من الفينولات (Kocot et al.,2018)&( Rzepecka-Stojko et al.,2016) إن وجود مجموعات الفينول في جزيئات الفلافونويدات يمنحها نشاطًا مضادًا للجذور الحرة. الأحماض الفينولية هي مركبات تحتوي على مجموعات كربوكسيلية وفينولية.
وضح ) Rahul et al.(2023عند دراستهم للغذاء الملكي الهندي بأن Apis mellifera وهو نوع نحل ثمين معروف بإنتاجه لمجموعة متنوعة من المنتجات الغذائية وهناك عوامل تؤثر عليه مثل نوع النحل والبيئة والموسم وتقنية الجمع وعمر اليرقات على تكوين غذاء ملكات النحل الهندي على المستويين الكلي والجزئي تم دراسة المعايير الفيزيائية والكيميائية لعينات غذاء ملكة النحل الهندي التي جمعت من المناطق الجنوبية والوسطى والشمالية من الهند واختبار نشاط مضادات الاكسدة والقوة الاختزالية حيث اظهر غذاء ملكة النحل من المنطقة الوسطى اظهر افضل فعالية للقوة الاختزالية واعلى محتوى بوليفينولي.
5-3- ربط آيون الحديدوز Ferrous ion binding
يمتلك غذاء ملكة النحل عدد من المواد الفعالة التي لها القدرة في منع عمليات الأكسدة إذ إنها يمكن ان تساهم في تحول آيون الحديد من الشكل Fe3+ الى الشكل Fe2+ حيث يعد الأخير الشكل المستقر لآيون الحديد وذلك ناتج بفعل المركبات المانعة للأكسدة إذ تعمل على وهب الكترون او أنتزاع بروتون من الشكل غيرالمستقر لآيون الحديد (Yen et al.,2005).
بين Kedare and Singh(2011) بأن اختبارات الاكسدة تستخدم على نطاق واسع لتقييم نشاط مضادات الاكسدة في مختلف المنتجات الطبيعية حيث يستخدم اختبار ربط ايون الحديدوز لمضادات الاكسدة كعوامل اختزال في طريقة قياس لونية مرتبطة بالاكسدة والاختزال باستخدام مادة قياسية مؤكسدة سهلة الاختزال. للمصادر الزهرية وتنوعها وطبيعة الأغذية التي تستعمل في تغذية النحل ينعكس على طبيعة ونسب المركبات ذات الخصائص المانعة للاكسدة في منتجات النحل مثل الفينولات والمواد الفعالة الأخرى وبالنتيجة تنعكس على قابلية ربط آيون الحديدوز (Perez et al.,2013). نظرا” لكثرة الاقبال المتزايد على استخدام غذاء ملكة النحل كمغذي واستخدامه كعلاج لذلك وجب أن يكون غذاء ملكة النحل المتناول عالي الجودة لذلك درس ( ( Pavel et al.,2014الخصائص الفيزيائية والكيميائية ونشاط مضادات الاكسدة وقارن بين عينات غذاء ملكات النحل الطازجة المحلية التي تم الحصول عليها مباشرة من النحالين والعينات التجارية حيث كشفت النتائج وجود ارتباط بين قوة مضادات الاكسدة المختزلة للحديديك ونشاط إزالة الجذور الحرة (DPPH) ومجموع البوليفينولات وكانت اعلى بكثير في عينات غذاء ملكة النحل المحلية وهذا يدل على جودة غذاء ملكة النحل المحلي مقارنة” بالعينات التجارية. درس (Balkanska et al. (2017 النشاط المضاد للأكسدة في غذاء ملكة النحل RJ الذي تم جمعه من منطقتين في بلغاريا ( Lovech و (Veliko Tarnovo وعينات غذاء ملكي تم شراءه من السوق المحلي واختبرت قوة مضادات الاكسدة المختزلة للحديديك حيث أظهرت كل من قوة ربط ايون الحديدوز والبوليفينولات الكلية تباينا” واضحا” من حيث الارتباط فيما بينهما. يتأثر التركيز الكلي للمركبات الفينولية في غذاء ملكة النحل بعوامل عديـــــدة مثـــل نوع النبات وصحتــه والموســــــم والمنــــاخ حيـــث درس (Takruri and Alkhedr.2021) القدرة الكلية لمضادات الاكسدة باستخدام أختبار ربط الحديدوز حيث تعمل القدرة الاختزالية لــ FRAP قدرة مضادات الاكسدة في RJ والعسل على اختزال Fe+3+ إلى Fe+2 وتستخدم هذه الطريقة (ربط آيون الحديدوز ) بسبب قدرتها على توفير نتائج أكثر دقة لمضادات الأكسدة في غذاء ملكة النحل والعسل.
6- تشخيص السكريات بواسطة جهاز Diagnosis of Sugers by HPLC-RI
حددت السكريات الرئيسية الثلاثة في غذاء ملكات النحل (الفركتوز والكلوكوز والسكروز) بالإضافة الى نسبة قليلة من المالتوز وتم تطوير طريقة كروماتوغرافيا السائل عالية الأداء (HPLC) مع كشف معامل الانكسار (RID) لتحديد السكر في غذاء ملكات النحل وتعتبر هذه الطريقة ذات حساسية كافية ولا تعاني من تداخل المصفوفات وتظهر قابلية تكرار جيدة (Sesta,2006).
تشكل السكريات وخاصة السكريات الثلاثة الرئيسية حوالي (18-52%) من الوزن الجاف بينما تشكل (6-18%) من العينة الطازجة و شهدت الفترة الأخيرة نموا” ملحوظا” في استهلاك غذاء ملكة النحل بسبب قيمته الغذائية العالية ومكوناته النشطة ولأن سعر غذاء ملكة النحل اعلى بكثير من منتجات النحل الأخرى مما جعله عرضه للغش التجاري لذلك درس (Balkanska,2018) توصيف تركيبة السكر في غذاء ملكة النحل المغشوش بغذاء ملكات النحل والعسل لكي يتم تحديد الاوصاف المحتملة للغذاء الملكي المغشوش والكشف عن عمليات الغش بسهولة . وظهرت من خلال الدراسة وجود فروق كبيرة في محتوى الفركتوز والكلوكوز والسكروز بين غذاء ملكة النحل النقي والمخلوط ومن خلال النتائج يمكن استخدام معايير الفركتوز والكلوكوز كأوصاف جيدة لتقييم غذاء ملكة النحل النقي. وجد أن السكر الأكثر وفرة في عينات غذاء ملكة النحل هو الفركتوز وهو اعلى بخمس مرات تقريبا من عينات غذاء ملكة النحل المخلوط. من اهم الممارسات التي يتبعها النحالون خلال انتاج غذاء ملكة النحل هي التغذية الصناعية بالسكر حيث بين (kanelis et al.,2018)بأنه من خلال الدراسات تم اكتشاف تأثير التغذية الصناعية بالسكر على تركيب السكريات الرئيسية الثلاثة (الفركتوز والكلوكوز والسكروز) في غذاء ملكة النحل بلغ متوسط إنتاجية المستعمرة الواحدة غير المُضافة (المجموعة أ) 12.8 غرام، بينما بلغ متوسط محتوى الفركتوز والكلوكوز والسكروز 4.32% و3.78% و0.04% على التوالي وبالنسبة للمستعمرات التي تم تغذيتها في يوم التطعيم مرة واحدة (المجموعة ب)، كانت هذه القيم 12.76 غم ، 3.11%، 3.19% و3.71%، وبالنسبة لمستعمرات النحل التي تم تغذيتها حتى يوم الجمع (المجموعة ج) كانت 12.81 %، 3.05%، 3.12% و3.54% على التوالي. تجدر الإشارة أيضًا إلى أن محتوى السكروز في جميع عينات مستعمرات النحل المُضاف إليها العلف كان أكبر من 1.97%، أظهرت الاختبارات الإحصائية تأثير التغذية الاصطناعية على محتوى الفركتوز والكلوكوز بينــما ظلت الكميـــة المُنتجة دون تأثير. يعد تحديد محتوى السكر في عينات العسل وغذاء ملكة النحل امرا” بالغ الأهمية لتقييم جودتها وللسكريات دور مهم في تعزيز وتنظيم المسارات الأيضية للدهون والكربوهيدرات كذلك يمكن استخدام السكريات كمعيار للتحقق من الغش التجاري من خلال التأكد من وجود السكريات الرئيسية الثلاثة (الفركتوز والكلوكوز والسكروز) والتي تشكل نسبة (7-18%) من اجمالي المكونات الأخرى للغذاء الملكي. وهناك عدة عوامل تؤثر على تقييم مستوى السكريات الرئيسية والثانوية مثل تنوع المنشأ وموسم الحصاد ونظام تغذية النحل واستخدمت عدة طرق مختلفة لتحديد محتوى السكر في غذاء ملكة النحل بما في ذلك كروماتوغرافيا الغاز والتي تتطلب مرحلتي تنقية واشتقاق إضافة الى طريقة أخرى انزيمية تحدد كل نوع من السكر على حدة، لذلك تم تطوير تقنية غير الطرق السابقة وتعتبر اكثر دقة وبسيطة وهي كروماتوغرافيا السائل عالي الأداء (HPLC) لتحليل ثلاثة أنواعٍ من السكريات (الفركتوز والكلوكوز والسكروز) في غذاء ملكة النحل اضافة الى الكشف عن السكريات الأخرى مثل المالتوز والذي يعتبر وجوده دلالة على الغش بالسكروز وتتطلب طريقة كروماتوغرافيا السائل عالي الأداء لتحليل السكروز الحاجة إلى تحضير العينة لإزالة الدهون والبروتينات قبل بدء التحليل (2024 (Alkindi et al.,.
7 -الفعالية الانزيمية في غذاء ملكة النحل Enzymatic activity in royal jelly
تعتبر الإنزيمات من العناصر الأساسية في منتجات نحل العسل وتستخدم كمؤشر على درجة التسخين في بعض الدول. يتم إفراز هذه الإنزيمات بواسطة شغالات النحل من الغدد تحت البلعومية وخاصة تلك التي تجاوز عمرها 21 يومًا. تشمل هذه الإفرازات إنزيمات الإنفرتيز والدياستيز والكلوكوز- أوكسيديز وتلعب هذه الإنزيمات دورًا مهمًا في إنضاج الرحيق وتحويله إلى عسل حيث يحتوي العسل الناتج على هذه الإنزيمات ما لم تتعرض للتلف نتيجة التسخين أو التخزين في درجات حرارة مرتفعة (العريفي، 2010) يوجد في العسل وغذاء ملكة النحل العديد من الإنزيمات، بعضها يأتي من النباتات والبعض الآخر من شغالات نحل العسل، ومنها:
– 1-7 الفعالية الإنزيمية لإنزيم الدياستيز Diastase activity Assay
الدياستيز هو الاسم الشائع لإنزيم يُسمى ألفا أميليز. يتمثل دور هذا الإنزيم في تفكيك الكربوهيدرات المعقدة مثل النشأ إلى سكريات يسهل استقلابها. يُضيف النحل الدياستيز إلى الرحيق أثناء التغذية ولكن نظرًا لعدم وجود نشأ في الرحيق. عند افراز الانزيمات وخصوصا” الدياستيز من قبل النحل العامل يصعب عليه بعد ذلك التخلص من الانزيم لذلك تفرز الانزيمات في العسل الناتج حيث يُحفظ لفترات طويلة. يتأثر انزيم الدياستيز بالحرارة والتسخين ويؤدي ذلك الى توقف عمله لذلك يُمكن استخدامه كمقياس غير مباشر لنضارة عينة العسل ويقيس اختبار الدياستيز سرعة انقسام جزيئات النشا بواسطة إنزيم معين موجود في العسل والحد الأدنى لنشاط الدياستاز وهو 8.0 DN (2019 Howse, Jaine and ).
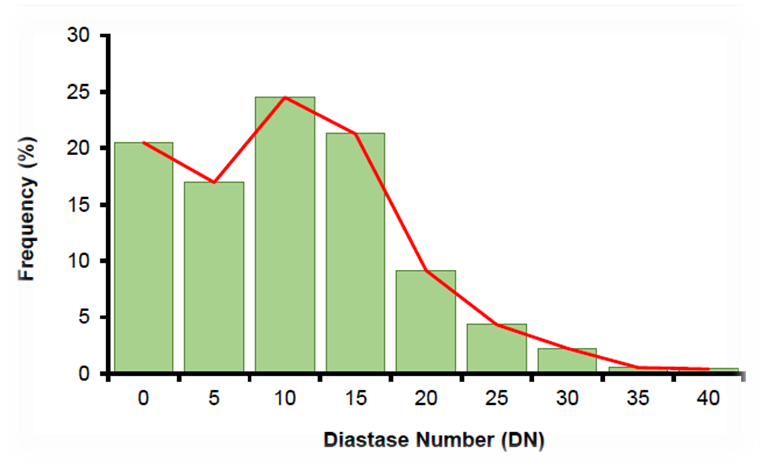
شكل (4) تمثل تكرار النشاط الدياستيزي في أنواع العسل النيوزيلندي (2019 Howse, Jaine and ).
يُعتبر تقدير الدياستيز في العسل وغذاء ملكة النحل من الصفات الأساسية التي تعكس جودته العالية حيث يلعب دورًا مهمًا في تحفيز تحلل الكربوهيدرات إلى سكريات بسيطة مثل تحويل النشا إلى دكسترينات وسكريات أحادية وثنائية وسكريات قصيرة السلسلة (Oligosaccharides) يُظهر نشاط الدياستيز الظروف المثلى لتخزين منتج العسل مما يدل على عدم تعرضه للحرارة وبالتالي يشير إلى طزاجة العسل أو تعرضه للتسخين المفرط ويُعتبر هذا المعيار من الأسس الرئيسية في تقييم طزاجة العسل كما يُستخدم كمؤشر على نقاوته وعدم غشه بالسكريات، حيث أن المصدر الرئيسي له هو النحل العامل بالإضافة إلى حبوب لقاح الأزهار (Yilamaz and Kufrevioglu, 2001). يعبر عنه بالرقم الدياستيزي Diastase number (DN) ويجب أن لا يقل محتواه عن 8 وحدات في منتجات النحـــل بحسب الموصفات الأوربية.(Bogdanov, 2009) European Standards
يتم التعبير عنه بوحدة Schade unit : وهي كمية الإنزيم اللأزمة لتحويل 0.01 من النشا الى نقطة النهاية خلال ساعة واحدة عند درجة 40 مْ تحت ظروف الاختبار .(Muli et al., 2007)
توصل سلمان،(2019) عند دراسته لنماذج من العسل العراقي من مناطق مختلفة وجد بأن اعلى قيمة حصل عليها كانت من عسل محافظة البصرة والتي كانت بحدود (14.36 وحدة) في حين كانت محافظة بابل هي الأقل قيمة وكانت (.67 8 وحدة).
وأيضا وجد (Taha,(2020 عند دراسته لأصناف من العسل المصري ان قيم DN لجميع العينات كانت اقل من الحد القياسي الموصى به كذلك أوضح أن فعالية إنزيمات العسل بما في ذلك الدياستيز تتأثر بعدة عوامل مثل مصدر الغذاء والتقنيات المستخدمة في جمع العسل بالإضافة إلى ظروف التخزين حيث يُعتبر نشاط الإنزيمات مؤشرا“ على نضج العسل بعد تحويله من الطور الرحيقي.
قدر ( Xagoraris et al., (2021 قيم النشاط الدياستيزي بحدود (11.1-51.1 وحدة ) عنــد دراسة عينات من العسل اليوناني أحادية المصدر الزهري. درس( Tomczyk et al., (2022 الرقم الدياستيزي لأصناف من العسل البولندي جمعت من مناطق مختلفة ومتنوعة الغطاء النباتي ووجد بأن قيم رقم الدياستيز تراوحت بين 15.16 – 28.25 وحــــدة حيث أشار الى ان التحولات الكيميائية التي تحدث للرحيق الزهري داخل جوف عاملات النحل يرافقه تحول للنشأ ولكن بنسب اكبر مما هو في العسل.
7-2- الفعالية الإنزيمية لإنزيم الأنفرتيز Invertase activity Assay
يعتبر غذاء ملكة النحل من المنتجات الحيوية الغنية بالانزيمات ومنها انزيم الانفزتيز الذي يعد من الانزيمات المهمة التي تتواجد في تركيب غذاء ملكة النحل نظرا” لدوره في التحلل الحيوي للسكريات المعقدة وتحسين القيم الغذائية للغذاء الملكي (Ramadan and Al-Ghamdi,2012). الإنفرتيز (Invertase) هو الإنزيم المسؤول عن العديد من التغيرات الكيميائية التي تحدث أثناء إنضاج الرحيق وتحويله إلى عسل ويُعتبر هذا الإنزيم من إنزيمات التحلل المائي الذاتي (Hydrolysis) حيث تضيفه عاملات النحل إلى الرحيق حيث يلعب الإنفرتيز دورًا أساسيًا في تحويل السكروز إلى جلوكوز وفركتوز بالإضافة إلى دوره المهم في تحويل مجموعات D-Fructofuranose إلى وحدات من سكر D-Fructose والعديد من السكريات الأحادية الأخرى(عويس,2018). يعتبر نشاط الإنفرتيز أكثر حساسية للحرارة مقارنة بالدياستيز لذا فإن تقدير فعاليته يعد أمرًا بالغ الأهمية لتحديد جودة منتجات نحل العسل حيث بين ( العريفي ،2010) ان مستوى نشاط أنزيم الإنفرتيز في العسل يجب أن لايقل عن 40 وحدة / كغم.
بينت الدراسات أن نشاط انزيم الانفرتيز في العسل ينخفض بسكل ملحوظ عند تخزينه في درجات حرارة مرتفعة لفترات طويلة ويشير ذلك الى أهمية ظروف التخزين في الحفاظ على نشاط الانزيمات في منتجات النحل حيث توصل Flanjak et al. (2016) عند دراسته للعسل الكرواتي مختلف المصادر الزهرية حيث بلغ متوسط نشاط انزيم الانفرتيز لكل من أصناف العسل المدروسة حيث بلغ متوسط نشاط انزيم الانفرتيز 52.1 و94.7 و155.2 و 176.1 وحدة/كغم على التوالي.
كما اشارت دراسة أجريت من قبل Boussaid et al. (2018) على ستة عينات من العسل من مصادر نباتية وجغرافية مخلتفة في تونس وتبين بأن متوسط قيم نشاط انزيم الانفرتيز 84.68، 52.29 ، 46.25، 92.66 ، 73.74 و 82.01 وحدة \كغم لكل العينات المدروسة حيث كان للموقع الجغرافي ونوع النبات تأثير في تفاوت نسب النشاط الانزيمي بين أنواع العسل الستة.
درس (Al-Rubaie and Al-Fekaiki.(2022 تأثير ظروف التخزين والتسخين على نشاط الدياستيز والانفرتيز في نماذج العسل من مختلفة المناطق العراقية حيث وجدوا بأن نشاط انزيم الانفرتيز في عينات العسل المدروسة بلغت 107.5-284.3 وحدة/كغم وعند الخزن والتسخين في درجات حرارية مختلفة لفترات طويلة لوحظ وجود تغيرات في قيم النشاط الانزيمي حيث انخفض نشاط انزيم الانفرتيز الى 26.8-70.8 وحدة/كغم بعد التعرض للتسخين والتخزين لفترات طويلة .
بين (2024) Jembrek and Oršolićعند دراستهم للخصائص البيولوجية والفوائد الصحية لغذاء ملكة النحل بأنه يحتوي على تركيبة واسعة من المكونات الكيميائية والمجاميع الفعالة ومن ضمن تركيبته يحتوي على الانزيمات المهمة منها الاميليز والانفرتيز والكاتليز والفوسفاتيز الحامضي وغيرها من الانزيمات الأخرى.
8- كروماتوكرافيــا الغـــــاز المقتـــــرن بمطيــــاف الكتلــــة
Gas Chromatography-Mass Spectrometry (GC-MS)
يتكون جهاز كروماتوغرافيا الغاز ذو مطياف الكتلة (GC-MS)من مكونين أساسيين هما جهاز الكروماتوغرافيا ومكشاف طيف الكتلة ويكون الطور المتحرك في هذا الجهاز عبارة عن غاز خامل مثل ( الهليوم او النتروجين او الأركون) يتم ضخه الى الجهاز عن طريق أسطوانة مضغوطة ويتم التحكم في معدل سريانه من خلال عمود الفصل من خلال منظم الضغط وعادة” تستخدم الاعمدة الشعرية التي تختلف عن بعضها البعض بالطول والقطر وسماكة الطبقة الداخلية للطور الثابت تثبت على الجدار الداخلي للعمود ويتراوح طوله من 20-100 متر وقطره أجزاء من المليمتر ويتم صناعته من معدن خاص غرفة الفرن تتضمن عمود الفصل الذي يتم من خلاله التحكم في درجة الحرارة ضمن برنامج حراري مخصص لهذا الغرض وبالتالي تتحول المواد في العينة المحللة الى الحالة الغازية ثم فصلها يتم حقن العينة منم خلال أنبوب الحقن الموصول بفتحة الحقن في اعلى العمود ويتم نقل العينة من خلال الغاز الخامل عبر العمود يتم فصلها استنادا” الى اختلاف معاملات التوزيع بين الطورين الثابت والمتحرك إضافة” الى عوامل أخرى مثل درجة الحرارة المستخدمة وقابلية تطاير المادة المتحللة ويمتاز عمود الفصل بأنه يحتفظ بمواد العينة اعتمادا” على خصائصها وتخرج منه بعد زمن الاحتجاز الذي يكون مميزا” لكل مادة (Weber.et.al.,2007;Eiceman,2000).بعد ان يتم فصل المركبات في العينة تخرج من عمود الفصل ليتم وتصل الى مطياف الكتلة MS ويتم تأيينها وتحويلها الى شوارد بعدة تقنيات مثل التأين الكيميائي والتصادم الالكتروني ويقوم الكاشف بتحديدها وتعريضها لعملية التشظي ومن ثم يتم تحديدها اعتماداد على معدل الكتلة الى الشحنة لكل مادة علما” بأن الكاشف يكون حساسا” للتراكيز المنخفضة. (Adlard.and Handley. 2001)
بين (Ghadimi-Garjan et al.,(2023 عند دراسته مكونات غذاء ملكة النحل الطازج وغذاء ملكة النحل المجفف بالتجميد عند ضغط ودرجة حرارة 100 باسكال و-70 درجة مئوية حيث أشار تحليل كروماتوغرافيا الغاز- مطياف الكتلة (GC-MS) إلى أن كمية حمض 10-هيدروكسي-2-ديكانويك (10H2DA) في غذاء ملكات النحل الطازج كانت أعلى بمقدار 3.85 مرة من تلك الموجودة في غذاء ملكات النحل المجفف بالتجميد .
درس et al.,(2023) Yu تركيب غذاء ملكة النحل من الاحماض الدهنية وطرق الاستخلاص حيث وجد بأن الغذاء الملكي غني بالاحماض الدهنية التي لها تأثيرات وقائية وانشطة مناعية للصحة حيث بين بأن الاحماض الدهنية تشكل حوالي 80-85% من نسبة الدهون في الغذاء الملكي وهناك مجموعة واسعة من الاحماض الدهنية التي توجد في الغذاء الملكي.
9- التحليل الطيفي بالأشعة تحت الحمراء باستخدام تقنية FTIR
تضمنت هذه الدراسة تحليل أطياف غذاء ملكة النحل باستخدام FTIR حيث تم تسجيل مدى واسع من الاطياف تقع ضمن النطاق (4000-600 سم-1) حيث تعبر منطقة التمدد (3600-3000سم -1) عن المحتوى المائي ومجاميع الهيدروكسيل في الكربوهيدرات ومجاميع الأمين في البروتينات بينما تمثل منطقة التمدد (3000-2800 سم -1) تمثل كمية الدهون في العينة كما تمثل منطقة التمدد (1800-1600 سم -1) بالبروتينات في حين تعتبر منطقة التمدد (1300-900 سم -1) منطقة الكربوهيدرات ومنطقة التمدد التي اصغر من 800 سم -1 فتسمى منطقة بصمة الاصبع والتي تكون مزيج من المكونات الصغيرة والمجاميع الوظيفية. تم التحقق من النتائج باستخدام HPLC-PDA ولوحظ وجود تشابه بين نتائج FTIR و HPLCالى حد كبيــر لذلك يمكن استخدام تقنية التحليل الطيفي FTIR المتطورة للتنبؤ بسرعة وسهولة ودقة بمحتوى غذاء ملكة النحل في منتجات خلية النحل.( Cebi et al.,2020) .وشهدت الآونة الأخيرة اهتماما كبيرا” بمنتجات النحل والتي تشمل العسل وغذاء ملكة النحل وحبوب اللقاح والبروبلس لكون هذه المنتجات استخدمت في عدة مجالات طبية وتغذوية وأثبتت فعاليتها في مقاومة الامراض وزيادة المناعة والخ من فوائد أخرى لاتعد ولا تحصى لذلك اتجهت انظار الباحثين والمهتمون بمجال النحل الى دراسة كل من هذه المنتجات ومعرفتها تركيبها الكيميائي والمركبات الحيوية التي أعطت تلك الأهمية لمنتجات النحل إضافة الى الاهتمام بالتحقق من ألاصل الزهري للعسل وبقية المنتجات. وبصورة عامة بين (Castiglioni et al. (2019 & (Kasprzyk et al. (2018 بأنه تم استخدام العديد من الطرق الفيزيائية والكيميائية ووجد بأن جميعها تحتوي على الرطوبة والرماد والسكريات والدهون والبروتينات والاحماض الامينية والعناصر المعدنية الأ ان الباحثون والمختصون بهذا المجال لم يكتفوا بهذه الطرق المتاحة لكونها تستغرق وقتا“ طويلا“ مما تطلب اكتشاف طرق علمية موثوقة وسريعة ودقيقة لتطوير هذا المجال لذلك تم إيجاد تقنية تتمتع بهذه المزايا المذكورة وهي تقنية التحليل الطيفي بالأشعة تحت الحمراء FTIR ويعتبر مطياف الاشعة تحت الحمراء بتحويل فورييه من اكثر طرق التحليل استخداما لتحديد المجاميع الوظيفية وهي تقنية تمتاز بسرعتها وغير مدمرة لتركيب مكونات الخلية الحيوية ويوفر معلومات حول الشظايا الجزيئية ووجود أو غياب مجموعات وظيفية محددة كذلك يسمح مطياف الاشعة تحت الحمراء بتقنية تحويل فورييه مع وحدة ART بتخفيف الاشعاع الساقط بدون امتصاص المحتوى المائي للمركب للعينة وتم استخدام هذه التقنية بطرق مختلفة منها FTIR-ATR لغرض تحليل مكونات منتجات النحل وهي تقنية حساسة جدا” عند تحليل العينات مما يعطي نتائج موثوقة وعلمية وأيضا يمكن استخدام مطيافية التحليل لتوصيف بنية وتركيب غذاء ملكة النحل والمنتجات الأخرى.
(Hospodarova et al.,2018)& (2015 ,Anjos et al.) &(2013(Jandrić et al.,.
بين (Rassu et al., 2015) بأنه كل قمة متكونة تشير إلى نطاق محدد يمثل المركب الكيميائي المرتبط بها. على سبيل المثال، تعبر القمة الموجودة في النطاق 3275 سم⁻¹ عن تمدد مجموعات O-H الناتجة عن اهتزازات منطقة تمدد الماء وN-H من الأمينات. أما النطاقات عند 1800 سم⁻¹ و1636 سم⁻¹، فهي تمثل الأميد I وترتبط باهتزازات تمدد C=O الناتجة عن تكوين البنية الهيكلية للبروتينات. في حين أن النطاق عند 1547 سم⁻¹ يمثل اهتزازات انحناء N-H وتمدد C-N للأميد II توفر هذه النطاقات معلومات قيمة عن التركيب الثانوي للبروتين.
10- ببتيدات غذاء ملكة النحل Royal Jelly Peptides of
تلعب الببتيدات دورا“ مهما“ في صحة الانسان من حيث تأُثيرها على القلب والاوعية الدموية والجهاز الهضمي والغدد الصماء وكذلك الجهاز العصبي والمناعي إضافة“ الى عملها كمضادات للأكسدة Antioxidants والاحياء المجهرية Antimicrobial (Sánchez and Vázquez, 2017) وكذلك يكون غذاء ملكة النحل ذا تأثير مثبط لنمو الميكروبات ومضاد للالتهابات ومهدئ ومسكن ومضاد للسموم نتيجة احتوائه على الكثير من المركبات الحيوية ومنها الببتيدات (Szweda, 2017) لها دور مهما أيضا في تغذية الانسان وتعزيز المناعة وعلاج للأمراض المزمنة. ((Borutinskaite et al., 2018. تعرف الببتيدات بأنها جزء من البروتينات التي تعمل كمواد حيوية وتؤدي وظائف بيولوجية وتكون موجودة بشكل حر في مصادرها الطبيعية وتمتاز بالعديد من الخصائص الحيوية داخل جسم الانسان (Apostolopoulos et al., 2021.). نظرا“ لأمتلاك غذاء ملكة النحل خصائص وظيفية متعددة بسبب مكوناته النشطة بيولوجيا“ وأحد هذه المكونات هي بروتينات غذاء ملكة النحل الرئيسية (MRJPs) Major royal jelly proteinsالتي تعتبر عاملا“ رئيسيا“ في نمو ملكة النحل وتشكل حوالي (82-90% وزن/وزن) من بروتينات غذاء ملكة النحل ولكل نوع من هذه البروتينات وظيفة خاصة به . تفرز الببتيدات من الغدد البلعومية لعاملات النحل حيث يفرز النحل نوعا” خاصا” من الببتيدات يسمى Defensin-1 ويعتبر من البروتينات الرئيسية في غذاء ملكة النحل (MRJP) الذي يلعب دورا“ مهما“ في الحفاظ على صحة اليرقات ولهذا البروتين أهمية في كونه مضاد للبكتريا ومضاد للأحياء المجهرية لكونه من المضادات الحيوية الطبيعية ، كذلك يتنج النحل ثلاثة ببتيدات أخرى و يعتبر (Defensin) برويتن صغير ( ببتيد) له القدرة على شفاء والتئام الجروح حيث تم استخدام غذاء ملكة النحل في الطب البديل كطريقة تقليدية للمساعدة في التئام الجروح حيث قام العلماء في كلا“ من إيطاليا وسلوفاكيا بالعمل على تحليل غذاء ملكة النحل مختبريا” لأكتشاف سبب امتلاكه هذه الخاصية العالية في شفاء الجروح حيث قاموا بتنقية الببتيد وتسميته 1-Defensin.( .(Buttstedt et al., 2014& Berezow ,2017& Dumitru et al.,2022
أشار Valachova et al., (2016) ان تشخيص كمية الببتيد المشتق من النحل Defensin-1 يعتبر أسلوبا“ جديدا“ في مراقبة جودة العسل وغذاء ملكة النحل والتأكد من جودة المنتج ، يكتسب العسل وغذاء ملكة النحل فعاليته المضادة للأحياء المجهرية بفعل وجود المركب الحيوي Bee defensin-1 إضافة” الى توليد بيروكسيد الهيدروجين والضغط الأزموزي العالي بفعل السكريات وانخفاض قيمة الأس الهيدروجيني حيث أن Bee defensin-1 هو ببتيد النحل الذي يفرز من الغدد تحت البلعومية Hypopharyngeal glands للنحل ويعتبر عنصر من مكونات غذاء ملكة النحل ويسمى أيضا” Royalysin الذي يمتلك نشاطا“ مضادا“ للبكتــــريا الموجبة گرام Gram-positive bacteria مثــــل Bacillus subtilis و Staphylococcus aureus ((Szweda ,2017.
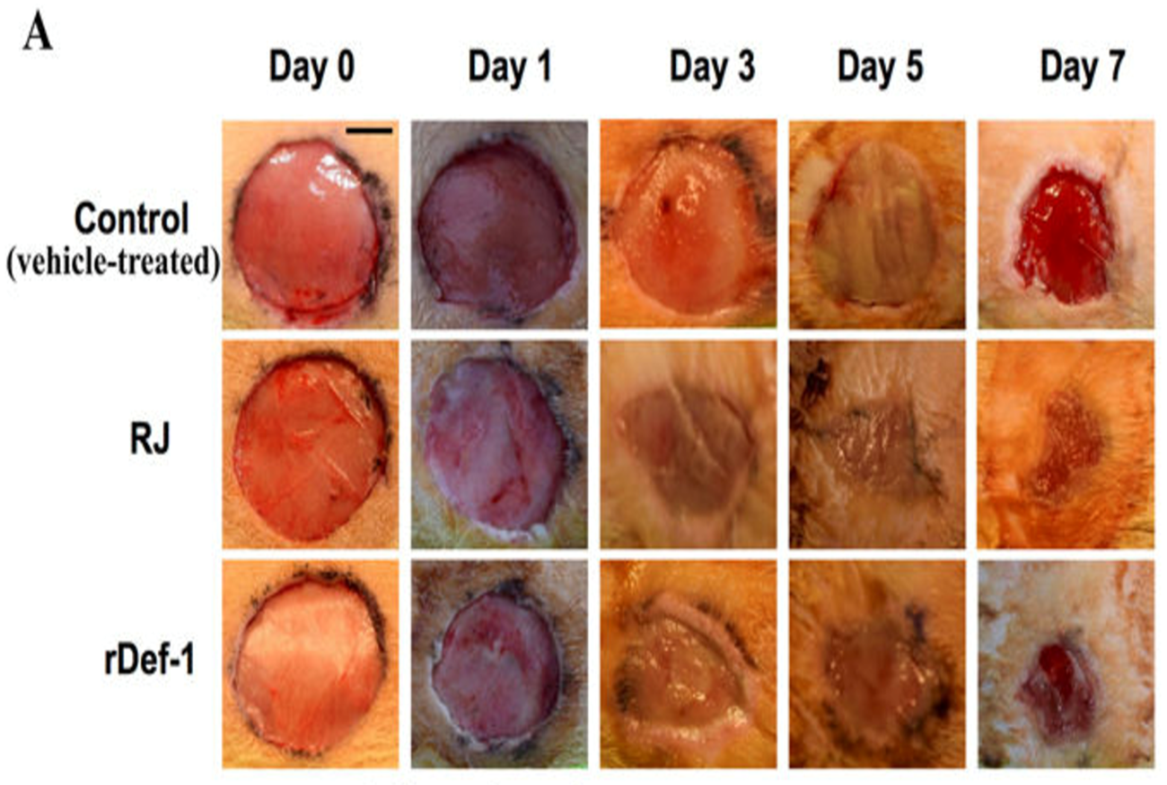
الشكل(5) دور الببتيد 1-Defensin في عملية شفاء الجروح (2017,Berezow)
- فصل وتنقية الببتيدات Separation and Purification of Peptides
تعتمد عملية فصل وتشخيص وتنقية الببتيدات الحيوية على سلسلة من الخطوات منفصلة واحدة عن الأخرى الخاصة بالتنقية التي تعتمد على الخواص الفيزيوكيميائية للببتيدات من حيث (حجم الجزيئات ، الشحنة الايونية، قابلية الذوبان، خواص الادمصاص وآلفة الارتباط مع الجزئيات الحيوية) لكي يتم فصل الببتيد عن المكونات الأخرى حيث أن عملية التنقية ضرورية قبل تحديد صفات البروتين او الببتيد وتعتمد طرق التنقية المتبعة على طبيعة المادة الأولية ويعد الاستخلاص اول خطوات عملية التنقية (Lee, 2017 & Pal and Suresh, 2016). تعتبر طرق فصل الببتيدات من الأغذية مهمة وصعبة، نظرًا لوجودها ضمن مزيج معقد يتكون من مواد متنوعة مثل الحوامض العضوية والأحماض الأمينية الحرة والسكريات والأملاح و تتطلب الدراسات التركيبية نقاوة عالية مما يجعل عمليات الفصل والتنقية بحاجة إلى تقنيات فعالة حيث تعتمد هذه التقنيات على فصل الببتيدات بناءً على الوزن الجزيئي بالإضافة إلى الخصائص الفيزيائية والكيميائية مثل كونها محبة أو كارهة للماء ويهدف هذا إلى الحصول على ببتيدات تتميز بالنقاوة وخصائص حيوية فعالة لذلك تُستخدم عادة تقنيات الكروماتوغرافيا وطرق الترشيح الفائق في عمليات التنقية (Sánchez and Vázquez, 2017)& (Cermeño et al., 2020).
11-1- كروماتوكَرافيا السائل عالية الأداء ذو الطور العكسيRP –HPLC
تم استخدام تقنيات الكروماتوغرافيا السائلة عالية الأداء ذات الطور المعكوس (HPLC-RP) في العديد من الدراسات والأبحاث الحديثة بهدف فصل وتشخيص المركبات الفعالة مثل البروتينات والببتيدات أصبحت هذه التقنية أداة أساسية في عملية فصل وتنقية البروتينات والببتيدات حيث يعتمد الفصل على خصائص الجزيئات الكارهة للماء تقوم هذه التقنية على إذابة العينة في مذيب مناسب (الطور المتحرك) ثم تمريرها عبر عمود الفصل، حيث يتم دفع الطور المتحرك بواسطة ضغط يتراوح بين 50 إلى 200 بار. ترتبط مكونات محلول العينة بدرجات متفاوتة مع محتوى تعبئة العمود (الطور الثابت) مما يؤدي إلى توزيع مكونات العينة بين الطورين بناءً على قطبيتها وتُعتبر تقنية RP-HPLC من أكثر أنواع HPLC استخدامًا في التشخيص والفصل حيث يكون الطور الثابت غير قطبي بينما يكون الطور المتحرك قطبيًا إذا كانت نسب الطور المتحرك تتكون من 1:1 من الماء وAcetonitrile فإن الفصل يتم تحت ظروف Isocratic (أي دون تغيير في مكونات الطور المتحرك). أما إذا تم استخدام نسب متباينة في مزيج المذيبات فيُطلق على هذه العملية اسم الغسل التدريجي (Gradient elution) أن جرى الفصل باستخدام نسب متباينة في مزيج مكونات الطور المتحرك ( Carr, 2020).
استخدم (2015). Mesaik et alكروموتوكرافيا السائل عالية الأداء ذات الطور المعكوس في فصل وتشخيص بروتينات وببتيدات العسل إذ استعمل عمود الفصل نوع C-18 Purospher STAR, RP-18 end-capped: 5 μm, 150-4.6, Merck, Darmstadt, Germany . وكذلك استعمل المذيبات: TFA، Acetonitrile والماء المقطر كطور متحرك . إذ تم تشخيص وجمع القمم المفصولة، من ثم تركيزها وحفظها على درجة حرارة 20 مْ لحين الاستعمال. تختلف المؤشرات الفيزيائية والكيميائية مثل اللون والرطوبة والحموضة بشكل ملحوظ بين عينات الغذاء الملكي مما يؤثر على خصائصها الحسية لذلك تُعتبر تقنيات الكروماتوغرافيا وسيلة فعالة لتصنيف منتجات النحل ويجب التركيز على تحديد بعض المكونات الثانوية المحددة (Escriche et al.,2017).
درس (Koike et al. (2020 فصل وتشخيص الببتيدات غير السامة في عسل النحل لتسعة ع درس (Koike et al. (2020 فصل وتشخيص الببتيدات غير السامة في عسل النحل لتسعة عشر عينة من مناطق مختلفة باستعمال تقنية كروموتوكرافيا السائل عالية الأداء واعتبرت هذه الطرق وسيلة للتحقق من سلامة منتجات النحل وجودتها.
11-2- عمود الفصل الكروماتوكرافي وآلية فصل الببتيدات
Chromatographic column and Mechanism of peptides separation
عمود الفصل في هذه التقنية يتميز بأن سطح حبيبات التعبئة تكون ذات خصائص كارهة للماء، وذلك نتيجة الارتباط الكيميائي لمجموعات الهيدروكربون بالسطح . يتم الاحتفاظ بالببتيدات من خلال عملية الامتزاز ويرتبط الجزء الكاره للماء من الببتيد بالسطح الكاره للما، كما هو موضح في الشكل (2-3). نظرا” لأن حجم الببتيدات كبير مقارنة بسماكة السطح الكاره للماء فإن جزءًا صغيرًا فقط من الببتيد يمتص على هذا السطح بينما يبقى الجزء الأكبر فوق السطح ويتفاعل مع الطور المتحرك يكون التفاعل الناتج عن هذا الامتزاز الكاره للماء قويًا مما يؤدي إلى بقاء الببتيد المدمص على السطح حتى يتم الوصول إلى تركيز معين من المذيب العضوي وبهذه النقطة يبدأ الببتيد المدمص في الخروج من العمود.
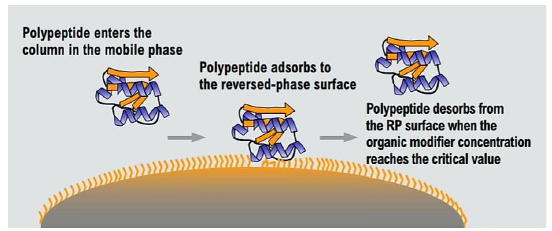
الشكل (6) أدمصاص القدم الكاره للماء للببتيد على السطح الكاره للماء في (Anonymous, 2011) RP-HPLC
تم استخدام كروماتوكرافيا السائل عالي الأداء ذو الطور المعكوس في فصل وتشخيص بروتينات وببتيدات العسل وايضا غذاء ملكة النحل بهدف توصيف الأنشطة المناعية لها، واستخدم عمود الفصل نوع C-18 (Purospher STAR, RP-18 end-capped: 5 μm, 150-4.6, Merck, Darmstadt, Germany وأيضا تم استعمال المذيبات- TFA – Acetonitrile) والماء المقطر) كطور متحرك. يتم تشخيص وجمع القمم المفصولة وتركيزها وحفظها بدرجة حرارة 20 مْ لحين الاستخدام Mesaik et al., 2015& Koike et al., 2020)).
11-3- الترشيح الهلامي Gel-filtration
تُعتبر تقنية الترشيح الهلامي واحدة من الطرق الفعّالة للفصل والتنقية وتعرف أيضًا باسم كروماتوغرافيا الاستبعاد الحجمي (Size-exclusion chromatography). تُعد هذه الطريقة سهلة الاستخدام لفصل الجزيئات ذات الأحجام الجزيئية المختلفة باستخدام ظروف فصل معتدلة. وتعتبر آلية فعّالة لفصل وتنقية الببتيدات بناءً على أحجامها الجزيئية حيث يتم تحديد عملية الفصل في الترشيح الهلامي وفقًا لحجم الجزيئات في المحلول المعــد تكون المكونات ذات الوزن الجزيئي الكبير غير قادرة على المرور عبر المسام الهلامية فتُستبعد إلى الخارج مع الحجم الميت (Void volume) بينما تدخل المكونات الصغيرة ذات الوزن الجزيئي المنخفض عبر المسام الهلامية وتبقى داخل عمود الفصل بعد ذلك يتم استبعادها إلى خارج الهلام بناءً على نوع الهلام المستخدم كما في الشكل (2-4 ) Cermeño et al., 2020)).
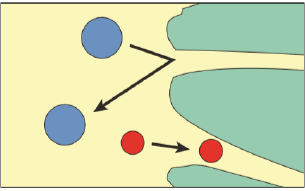
الشكل (7) ميكانيكية الفصل بالترشيح الهلامي (Anonymous, 2019)
قام Srisuparbh et al. (2003) بفصل وتنقية ببتيد Defensin-1 وهو بروتين مضاد للميكروبات موجود في غذاء الملكات (Royal jelly protein) الذي يلعب دورًا مهمًا في مكافحة البكتيريا بالتعاون مع المركبات الحيوية الأخرى الموجودة في العسل تم ذلك باستخدام تقنية الترشيح الهلامي على عمود كروماتوغرافيا Sephadex G-200 من طوائف نحل العسل A. cerena
استخدمet al. (2019) Bocianمجموعة من الخطوات لفصل وتنقية ببتيدات العسل المستخرج من سلالة Apis mellifera في جنوب شرق بولندا. شملت هذه الخطوات الترسيب باستخدام كبريتات الأمونيوم والأسيتون، بالإضافة إلى الفصل بواسطة كروماتوغرافيا الترشيح الهلامي باستخدام Sephadex G-25. بعد ذلك تم تقييم فعاليتها المضادة للأكسدة وللأحياء المجهرية.
نجح Ibrahim et al. (2021) في عزل وتنقية الببتيدات الفعالة حيوياً المستخرجة من البروتين الرئيسي للعسل، وذلك باستخدام تقنية كروماتوغرافيا الترشيح الهلامي تم ذلك من خلال استخدام عمود فصل كروماتوغرافي من نوع Sephacryl S-100 مع إجراء عملية شطف للعينة باستخدام محلول منظم Pyridine-acetate buffer بتركيز 12.5 ملي مولاري.
11-4- عمود الفصل GL 300/10Peptide SuperdexTM
يُعتبر عمود الفصل Column نوع GL 10/300PeptideTM Superdex عمودًا زجاجيًا مُعبأ مسبقًا ويُستخدم كأداة فعالة في تقنية الترشيح الهلامي حيث يوفر عمليات فصل سريعة ودقيقة ويتميز العمود بإجراءات جمع فعالة للأجزاء المستردة وهو مُعبأ بمادة Superdex التي تتكون من تقاطعات مستعرضة لجزيئات الأكاروز المسامية المرتبطة بالدكستران عبر روابط تساهمية. هذا التركيب يضمن وسطًا ثابتًا من الناحيتين الفيزيائية والكيميائية، ويعود هذا الثبات بشكل رئيسي إلى وجود التقاطعات المستعرضة. يعمل العمود على فصل الجزيئات الحيوية، مثل الببتيدات، التي تتراوح أوزانها الجزيئية بين 100 و9000 دالتون مع قدرة العمود على تحمل ضغط يصل إلى 18 بار..
AKTATM pure operating instructions, GE Healthcare Bio-Sciences) .).
– 12توصيف الببتيدات الحيوية Characterization of Bioactive Peptides
12-1- تسلسل الاحماض الامينية:
لاحظ إن الفعالية الحيوية للببتيدات (MPRJ1) المستخلصة من سلالات النحل Apis cerana تتضمن تتابعًا من الأحماض الأمينية في النهاية الأمينية (N-terminal sequence) كما يلي: N(S)-Ile-Leu-Arg-Gly-Glu-Ser-Leu-Asp-Lys. تعتبر الأحماض الأمينية الوحدات الأساسية التي تشكل السلاسل الببتيدية حيث تلعب دورًا مهمًا في تحديد خصائص الببتيدات الحيوية بما في ذلك نشاطها كمركبات مضادة للأكسدة وأيضًا نشاطها المضاد للميكروبات ويعتمد ذلك على نوع وتسلسل الأحماض الأمينية التي تتكون منها الببتيدات والبروتينات (Sánchez and Vázquez, 2017).
ذكر Bose et al. (2020) بأن ببتيدات غذاء ملكة النحل (Bee defensin-1) المعزولة والمنقاة من عسل النحل Apis mellifera بأستخدام تقنية الترشيح الفائق بالإضافة إلى تقنيات الكروماتوغرافيا بنشاط حيوي فعال في التقاط وتثبيط الجذور الحرة مما يمنع انتشارها بفضل وجود النهاية الأمينية الكارهة للماء في السلسلة الببتيدية ويمتلك الببتيد تسلسلا“ متتابع من الاحماض الأمينية ( N(S)-Ile-Leu-Arg-Gly-Glu-Ser-Leu-Asn-Lys-Ser-Leu-Pro-Ile-Leu).
تحتوي مجموعة البروتينات الأساسية في غذاء ملكة النحل MRJP على كميات كبيرة من الأحماض الأمينية الضرورية لبقاء ملكة النحل و أطالة عمرها. ويهدف هذا إلى التحكم في التفاعلات الفسيولوجية الفريدة لغذاء ملكة النحل وخاصةً تلك المرتبطة بالنموAhmad et al., 2020)).
ومن الأحماض الأمينية الأساسية التي تم تحديدها في MRJPs: الفالين، والهيستيدين، والأرجينين، والليوسين، والإيزوليوسين، والليسين، والميثيونين، والفينيل ألانين، والثريونين، والتريبتوفان. (Ramanathan et al., 2018)..
تحتوي مركبات MRJPs على ما بين 400 و578 حامضًا أمينيًا تتراوح الأوزان الجزيئية لها بين 45 و68 كيلو دالتون (Buttstedt et al., 2014) .
تظهر الأبحاث أن التنوع الجيني وأنواع النحل العسلي والعمليات الحيوية والتفاعلات البروتينية التي تحدث أثناء تخزين غذاء ملكات النحل تؤثر على الوزن الجزيئي ونقاط التساوي الكهربائي لبروتينات غذاء ملكات النحل – وهي معايير أساسية لتحديد نوع البروتين ( Qu et al., 2008&Santos et al., 2005 : Zhang et al., 2012) .
13-حامض 10-HAD
يعد حامض 10- هيدروكسي-2- ديسينويك ( حمض الهلام الملكي) من المواد الأساسية في تركيب غذاء ملكة النحل المحلية وهو حامض دهنـي غـير مشبــع وهــو المركب الأكثـر أهمية الذي له بعــض الخصائص المعززة للصحة والمعدلة للمناعة ومضاد للأورام ومضاد حيـوي ومنشط للأعصاب وفـي الأونـة الأخيــرة تـم اكتشاف تأثير مثبط لهذا المكون الدهنـي في الإشارات المناعية الفطريـة وعلى الرغـــم مــن تقــدم الدراســات وتعـــــــددها فــــي مجــال الإشارات المناعية الفطريـة الا ان دراسات قليلة بينــت تأثيـــره على الإشـــــــارات المناعيـــــة وتوصـلت الى اهــــداف علاجيــــة جديـــدة لعـــلاج اضطرابـــات المناعــــــة (et al.,2012 .(Sugiyama بينت الدراسة التي توصل اليها (et al.(2021 Collazo بأن هذا المكون الدهني يعتبر من المكونات الأساسية في تركيبة غذاء ملكة النحل لان له تأثيرات معززة للصحة وله تأثير وقائي ضد الاشعة فوق البنفسجية في جلد الانسان حيث أفادت الدراسات التي توصل لها الباحثون بأن بعض الادوية الحالية المستخدمة في علاج الأورام السرطانية لها تأُثيرات جانبية أضافة الى وجود بعض العيوب لذلك تم العمل من قبل الباحثون على إيجاد دواء جديد له كفاءة عالية وسميته منخفضة وليس له اثار جانبية لذلك درس العلماء مميزات وتأثيرات غذاء ملكة النحل RJ الذي تفرزه النحل العامل ووجدوا بأنه يتمتع بخصائص غذائية ودوائية فعالة نظرا“ لأحتواءه على كميات كبيرة من البروتينات والدهون والكربوهيدرات والفيتامينات إضافة الى وجود الاحماض الدهنية الحرة التي تحتوي على 8-12 ذرة كاربون ( أحادية وثنائية الكربوكسيل) والتي هي الدهون الرئيسية في غذاء ملكة النحل لذلك وجد بأن الحامض 10- هيدروكسي-2- ديسينويك اهم مركب دهني في تركيب غذاء ملكة النحل ومكون أساسي وتم تقييم تأثيراته المضادة للأورام منفردا“ او دمجه مع مادة سيكلوفوسفاميد (CP) لتقييم تـأثيره على الفئران المصابة بأورام أيرليخ الصلبة ) EST) حيث أدى علاج الفئران المصابة باستخدام 10-HDA بمفرده او مع مادةCP عن طريق الفم مرة واحدة يوميا“ لمدة أسبوعين بجرعات 2.5 و5 ملغم/كغم وخاصةً مع CP أدى إلى انخفاض ملحوظ في حجم الورم ومعدل تثبيطه وعلامات الورم (AFP مستوى ألفا فيتوبروتين و ومستضد الورم السرطاني الجنيني (CAE) في المصل ومستوى مصل الكبد والكلى و أكسدة الدهون في الورم LPO و أكسيد النيتريك NO ومستوى عامل نخر الورم ألفا (TNF-) وتحسين ملحوظ في مستوى إنزيمات مضادات الأكسدة GPx و إنزيم الكاتالاز CAT ومستوى التعبير عن الجينات المنظمة لموت الخلايا المبرمج caspase-3 و Bax لذلك وفقًــا لنتائـــج الدراســات الحالية أظهر 10-HDA بجرعات 2.5 و5 ملغ/كغ، وخاصةً بالاشتراك مع CP تأثيرات مضادة للأورام جيدة ضد EST في الفئران ويمكن التوصية به كعامل جديد أو بديل مضاد للسرطان ضد الورم ((Albalawi et al.,2021.
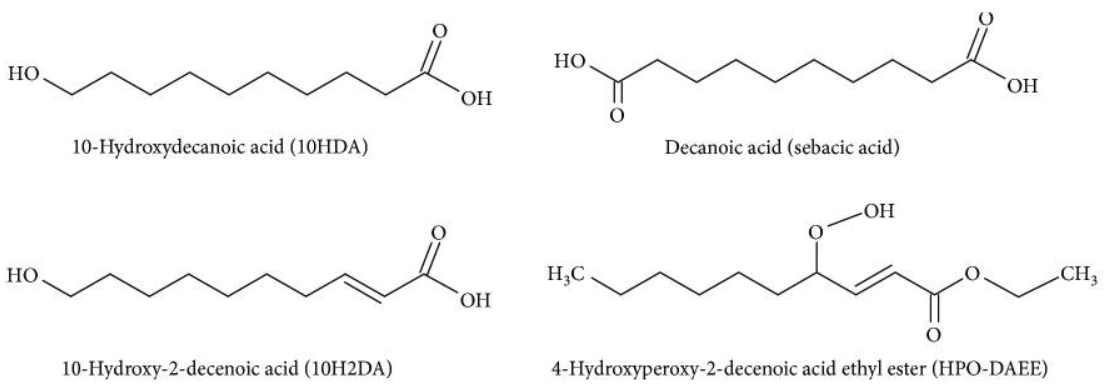
الشكل(8) الأحماض الكربوكسيلية في غذاء ملكات النحلet al.,2018) Kocot(
الخاتمة:
يُعد غذاء ملكة النحل من المنتجات الطبيعية الفريدة التي تتمتع بتركيب كيميائي غني ومتوازن، يمنحه خصائص غذائية وعلاجية متميزة. وقد أظهرت نتائج الدراسات السابقة أن لهذا الغذاء تأثيرات صحية متعددة تشمل تعزيز المناعة، ومحاربة الأكسدة، وتحسين وظائف الجسم الحيوية. كما يمثل غذاء ملكة النحل خيارًا واعدًا في مجال الطب البديل والتكميلي، خاصة لما يحتويه من مركبات نشطة مثل حمض 10-HDA والفيتامينات والأحماض الأمينية. ورغم هذه الفوائد، لا تزال هناك حاجة إلى إجراء المزيد من الدراسات السريرية والتجريبية لتحديد الجرعات المثلى، وفهم آلية تأثيره الحيوي بشكل دقيق، وضمان سلامة استخدامه على المدى الطويل. وعليه، توصي هذه المراجعة بتكثيف الجهود البحثية نحو استكشاف الاستخدامات المستقبلية لغذاء ملكة النحل وتطبيقاته في المجالين الغذائي والطبي.
النتائج:
- يحتوي غذاء ملكة النحل على نسبة عالية من الماء، البروتينات، الدهون، الكربوهيدرات، والمعادن.
- يتميز بوجود مركبات حيوية نشطة مثل حمض 10-HDA الذي يرتبط بتأثيرات مضادة للأكسدة والبكتيريا.
- يُظهر تأثيرات فسيولوجية إيجابية تشمل تقوية الجهاز المناعي، وتحسين الوظائف العصبية والتناسلية.
- له استخدامات علاجية في الطب البديل، ويدخل في العديد من المستحضرات الغذائية والطبية.
- تتأثر جودة الغذاء بعوامل عدة مثل نوع النحل، البيئة، طريقة التغذية، وطرق الجمع والحفظ.
التوصيات:
- إجراء دراسات سريرية وتجريبية لتقييم فعالية غذاء ملكة النحل بشكل علمي دقيق وآمن.
- تحديد الجرعات المثلى للاستخدام العلاجي والغذائي بناءً على الفئة العمرية والحالة الصحية.
- تطوير معايير جودة ومعايير قياسية عالمية لتداول وتخزين غذاء ملكة النحل.
- تشجيع البحث العلمي المحلي في البيئات العربية لدراسة تأثيرات الغذاء تحت ظروف مناخية وغذائية مختلفة.
- تعزيز الوعي الصحي لدى المستهلكين بأهمية وفوائد غذاء ملكة النحل وكيفية استخدامه بشكل آمن وفعّال.
المصادر
المصادر العربية:
العريفي، ابراهيم عبدالله. (2010).عسل النحل وخواصه الطبيعية والكيميائية والبيولوجية
والعلاجية. مكتبة الملك فهد الوطنية. ط 2 ، الرياض.
آسيا، بلفار. (2018). دراسة القدرة المضادة للأكسدة وللبكتيريا وللتآكل للمستخلصات الفينولية لنبات ( Limoniastrum guyonianum (Dur اطروحة دكتوراه. كلية الرياضيات وعلوم المادة.
سلمان، محمد علوان.( 2019). توصيف نماذج من العسل العراقي وتشخيص مركباتها الفعالة
ودراسة فعاليتها المضادة للأكسدة. اطروحة دكتوراه. كلية الزراعة. جامعة البصرة.
المصادر الأجنبية:
Adlard, E. R. and Handley, A. J. (2001). Gas chromatographic techniques and applications. London: Sheffield Academic.
Ahmad, S., Campos, M. G., Fratini, F., Altaye, S. Z., & Li, J. (2020). New Insights into the Biological and Pharmaceutical Properties of Royal Jelly. International Journal of Molecular Sciences, 21(2), 382.
Ahmed, M .; Shafiq, M.I .; Khaleeq, A.; Huma,R .; Abdul Qadir, M.; Khalhd, A.; Ali, A . and Samad, A. (2016). Physiochemical, biochemical, minerals content analysis,and antioxidant potential of national and Ineranational honeys in Pakistan. Journal of Chemistry. http//dx.doi.org/10.
Ajitha Nath K.G.R, Adithya Krishna S.B, Smrith. S, Jayakumaran Nair. A and Sugunan V.S.(2019). Biochemical Characterization and Biological Evaluation of Royal Jelly from Apis cerana. Journal of Food Technology and Food Chemistry: Volume 2 | Issue 1. ISSN: 2641-8118.
Albalawi, A. E., Althobaiti, N. A., Alrdahe, S. S., Alhasani, R. H., Alaryani, F. S., & BinMowyna, M. N. (2021). Anti-Tumor Effects of Queen Bee Acid (10-Hydroxy-2-Decenoic Acid) Alone and in Combination with Cyclophosphamide and Its Cellular Mechanisms against Ehrlich Solid Tumor in Mice. Molecules, 26(22), 7021. https://doi.org/10.3390/molecules26227021
Al-Kahtani, S., and El-Kazafy ,T. (2021). Effect of harvest time on royal jelly yield and chemical composition. Journal of the Kansas Entomological Society, 93(2). https://doi.org/10.2317/0022-8567-93.2.132
Alkindi .F , El–Keblawy .A , Ridouane. F and Mirza .SH.(2024). Factors influencing the quality of Royal jelly and its components: a review. Cogent Food & Agriculture. VOL. 10, NO. 1, 2348253. https://doi.org/10.1080/23311932.2024.2348253
Alkindi .F , El–Keblawy .A , Ridouane. F and Mirza .SH.(2024). Factors influencing the quality of Royal jelly and its components: a review. Cogent Food & Agriculture. VOL. 10, NO. 1, 2348253. https://doi.org/10.1080/23311932.2024.2348253.
Almeida-Muradian, L. B.; Barth, O. M.; Dietemann, V.; Eyer, M.; Freitas, A. S.; Martel, A.; Marcazzan, G. L.; Marchese, C. M.; Mucignat-Caretta, C.; Pascual-Maté, A.; Reybroeck, W.; Sancho, M. T. and Sattler, J. A. G. (2020). Standard methods for Apis mellifera honey research. J. of Apicultural Research, 59(3): 1–62.
Altun, S. K., and Aydemir, M. E. (2022). Determination of Antioxidant Capacities with the Phenolic and Flavonoid Contents of Royal Jelly Mixtures. Bee Studies- Apiculture Research Institute. https://doi.org/10.51458/bstd.2022.22.
Alzahrani, A. H.; Boukraâ, L.; Bellik, Y.; Abdellah, F.; Bakhotmah, B. A.; Kolayli, S. and Sahin, H. (2012). Evaluation of the antioxidant activity of three varieties of honey from different botanical and geographical origins. Global Journal of Health Science,3(4): 1- 6.
Anjos, O., Campos, M.G., Ruiz, P.C., & Antunes, P. (2015). Application of spectroscopy to the quantification( FTIR-ATR) of sugar in honey. Food Chemistry, 169, 218–223.doi:10.1016/j.foodchem.2014.07.138.
Anonymous (2011). Vydac® Reference Handbook Protein & Peptide Analysis and Purification. Grace Davison Discovery Sciences, 1-88. discoverysciences.com.
Anonymous (2019). Vydac ® 201TP and 202TP C18. HPLC columns, small molecule. Catalogue, MZ-Analysentechnik GmbH. 13 p. http://www.discoverysciences.com
Apostolopoulos, V.; Bojarska, J.; Chai, T.-T.; Elnagdy, S.; Kaczmarek, K.; Matsoukas, J.; New, R.; Parang, K.; Lopez, O. P.; Parhiz, H.; et al. (2021). Global Review on Short Peptides: Frontiers and Perspectives. Molecules, 26, 430.
Asaduzzaman., Rahman .S., Munira. S., Rahman .M.M., Islam .M. ,Hasan. M. ,Siddique .M .,Biswas .M .,Khan .M.,Rahman .M .and Belal.H.(2015). Analysis of Biochemical Composition of Honey and its Anti-Oxidant, Phytochemical and Anti-Bacterial Properties. Journal of Biomedical and Pharmaceutical Research Volume 4, Issue 4, July-August, 2015, 69-81. ISSN: 2279 – 0594.:
Aslan .A , Can .M.I ,Gok .O , Beyaz .S , Parlak .G and Ozercan .I.H.(2021). The inducing of caspase and bcl-2 pathway with royal jelly decreases the muscle tissue damage exposed with uoride in rats.Research Square https://doi.org/10.21203/rs.3.rs-447498/v1
Bagameri L, Baci G M and Dezmirean , D.S.(2022). Royal Jelly as a Nutraceutical Natural Product with a Focus on Its Antibacterial Activity. MDPI:
Bahar, E.; Ara, J.; Alam, M.; Nath, B.; Bhowmik, U. and Runi, N. (2013). In-vitro antioxidant and thrombolytic activity of methanol extract of Sida acuta. Journal of Pharmacognosy and Phytochemistry, 2 (2): 125-133.
Bahorun, T.; Soobrattee, M.A.; Luximon-Ramma, V. and Aruoma, O.I. (2006). Free radicals and antioxidants in cardiovascular health and disease. Internet Journal Medicine Update, 1:25-41
Bakchiche, B. (2017). Total Phenolic, Flavonoid Contents and Antioxidant Activities of Honey and Propolis Collected from the Region of Laghouat (South of Algeria). International Journal of Pharmacognosy & Chinese Medicine, 1(2). https://doi.org/10.23880/ipcm-16000110
Balkanska, R. (2018). Correlations of physicochemical parameters, antioxidant activity and total polyphenol content of fresh royal jelly samples. International Journal of Current Microbiology and Applied Sciences, 7(04), 3744–3750. https://doi.org/10.20546/ijcmas.2018.704.421
Balkanska, R. (2018). Correlations of physicochemical parameters, antioxidant activity and total polyphenol content of fresh royal jelly samples. International Journal of Current Microbiology and Applied Sciences, 7(04), 3744–3750. https://doi.org/10.20546/ijcmas.2018.704.42
Balkanska, R., Zhelyazkova, I., and Ignatova, M. (2012). Physico-chemical quality characteristics of royal jelly from three regions of Bulgaria. Agricultural Science and Technology, 4(3), 302–305. http://tru.uni-sz.bg/ascitech/3_2012/pqs_1 – physico-chemical quality characteristics of royal jelly.
Balkanska. R and Kashamov. B .(2011). Composition and physico-chemical properties of lyophilized royal jelly. ARI BİLİMİ / BEE SCIENCE;11(4):114-117.
Balkanska. R., Marghitas. L. and Pavel. C. I. (2017). Antioxidant Activity and Total Polyphenol Content of Royal Jelly from Bulgaria. International Journal of Current Microbiology and Applied Sciences, 6(10), 578–585. https://doi.org/10.20546/ijcmas.2017.610.071
Bazeyad, N. a. Y., Al-Ghamdi, N. a. A., & Alattal, N. Y. Z. (2022). Physicochemical characteristics of local royal jelly produced in Al-Baha region, Saudi Arabia. World Journal of Advanced Research and Reviews, 14(1), 284–292. https://doi.org/10.30574/wjarr.2022.14.1.0327
Berezow .A. (2017).A Molecule In Bees’ Royal Jelly Promotes Wound Healing . American Council on Science and Health.
Berezow .A. (2017).A Molecule In Bees’ Royal Jelly Promotes Wound Healing . American Council on Science and Health.
Bocian, A. ; Buczkowicz, J. ; Jaromin, M. ; Hus, K. K. and Legáth, J. (2019). An Effective method of isolating honey proteins. j. molecules, 24 (1): 1-10.
Bogdanov, S.(2009). Hamronised methods of the International Honey Commission. IHC responsible for the methods: Bee Product Science, http://www.bee-hexagon.net/en/network.htm
Borutinskaite, V.; Treigyte, G.; Čeksteryte, V.; kurtinaitiene, B. and Navakauskiene, R. (2018). Proteomic identification and enzymatic activity of buckwheat (Fagopyrum esculentum) honey based on different assays. J. of Food and Nutrition Research, 57(1): 57–69.
Bose, D.; Padmavati, M. and Banerjee, R. (2020). Isolation, purification and characterization of protein from Litchi chinensis honey and generation of peptides. J. of Addiction and Recovery, 3 (1): 1-6.
Buttstedt A.; Moritz R. F. A.; Erler S. (2014). Origin and function of the major royal jelly proteins of the honeybee (Apis mellifera) as members of the yellow gene family. Biological Reviews, 89: 255–269.
Capparucci, C., Gironi, F., & Piemonte, V. (2010). Equilibrium and extraction kinetics of tannins from chestnut tree wood in water solutions. Asia-Pacific Journal of Chemical Engineering, 6(4), 606–612. https://doi.org/10.1002/apj.455
Carr, D. (2020). A Guide to the Analysis and Purification of Proteins and Peptides by Reversed-Phase HPLC. ACE. HPLC Columns, 60: 1-64.
Castiglioni, S.; Astolfi, P.; Conti, C.; Monaci, E.; Stefano, M. and Carloni, P. (2019). Morphological, physicochemical and FTIR spectroscopic properties of bee pollen loads from different botanical origin. Molecules, 24:3974.Doi:10.3390/molecules24213974.
Cebi, N., Bozkurt, F., Yilmaz, M. T., & Sagdic, O. (2020). An evaluation of FTIR spectroscopy for prediction of royal jelly content in hive products. Journal of Apicultural Research, 59(2), 146-155 .
Cermeño, M.; Kleekayai, T.; Amigo-Benavent, M.; Harnedy-Rothwell, P. and FitzGerald, R. J. (2020). Current knowledge on the extraction, purification, identification, and validation of bioactive peptides from seaweed. Electrophoresis, 41, 1694–1717.
Chen ,Y.L and Zhang, J,(2015). Food Research and Development ,36 (2):148-152.
Cobzaru C., .2014. Natural Extracts: Particularities, Processes, Uses, Ed. PIM, Iasi.
Collazo, N. , Carpena, M. , Nunez- Esteve, B. , Otero P , Gandara J.S and Prieto M.A.(2021).Health Promoting Properties of Bee Royal Jelly: Food of e Queens. Nutrients 2, 13, 543
Cornara.L , Biagi. M , Xiao. J, Burlando .B.(2017). Therapeutic Properties of Bioactive Compounds from Different Honeybee Products .Frontiers: Volume 8. https://doi.org/10.3389/fphar.2017.00412
Cornelia, P. and Chis, A .(2011) . Chemical and biochemical characterization of three different types of honey from Bihor county. Analele Universitatii din Oradea , Fasicula: Ecotoxicologie, Zootehnie si Technologii de Industrie Alimentara. PP: 313-318.
Daniele, G. and Casabianca, H. (2012). Sugar Composition of French Royal Jelly for Comparison with Commercial and Artificial Sugar Samples. Food Chemistry, 134, 1025-1029.
https://doi.org/10.1016/j.foodchem.2012.03.008
Dimitrova, B.; Gevrenova, R. and Anklam, E.(2007). Analysis of phenolic acids in honeys of different floral origin by solid-phase extraction and high-performance liquid chromatography. Phytochemical Analysis, 18: 24-32. doi: 10.1155/2018/7074209
Dumitru, C. D.; Neacsu, I. A.; Grumezescu, A. M. and Andronescu, E. (2022). Bee-derived products: chemical composition and applications in skin tissue engineering. Pharmaceutics, 14, 750.
Eiceman, G.A. (2000). Gas Chromatography. In R.A. Meyers (Ed.), Encyclopedia of Analytical Chemistry: Applications, Theory, and Instrumentation, Chichester: Wiley.
Escriche, I.; Sobrino-Gregorio, L.; Conchado, A. and Juan-Borrás, M. (2017). Volatile profile in the accurate labelling of monofloral honey. The case of lavender and thyme honey. Food Chem., 226, 61–68.
El-Guendouz, S., Machado, A. M., Aazza, S., Lyoussi, B., Miguel, M. G., Mateus, M. C., & Figueiredo, A. C. (2020). Chemical characterization and biological properties of royal jelly samples from the Mediterranean area. Natural Product Communications, 15(2), 1934578X2090808 https://doi.org/10.1177/1934578×20908080
Faker El-Din H.M., El-Messery T.M., Mehanna N.S., Ali A.A-E., Hassan Z.M.R. and Amarowicz R.(2015). Interaction between some plants tannins and milk protein, Intern. J. Food Nutrit. Sci., 4 (1), 2015, 16-20.
Fattouch. S., Caboni, P.; Coroneo, V.; Tuberoso, C.I.G.; Angioni, A.; Dessi, S.; Marzouki, N. and Cabras, P. (2007). Antimicrobial activity of tunisian quince (Cydonia oblonga Miller) pulp and peel polyphenolic extracts. Journal of Agricultural and Food Chemistry, 55: 963-969.
Flanjak, I., Priomorac, L., Vukadin, I., Kovačić, M., Puškadija, Z., & Rajs, B. B. (2019). Physicochemical characteristics of Croatian royal jelly. Croatian Journal of Food Science and Technology, 11(2), 266–271. https://doi.org/10.17508/cjfst.2019.11.2.18.
Flanjak, I., Priomorac, L., Vukadin, I., Kovačić, M., Puškadija, Z., & Rajs, B. B. (2019). Physicochemical characteristics of Croatian royal jelly. Croatian Journal of Food Science and Technology, 11(2), 266–271. https://doi.org/10.17508/cjfst.2019.11.2.18.
Fratini .F , Cilia. G , Mancini .S and Felicioli .A.(2016). Royal Jelly: An ancient remedy with remarkable antibacterial properties. Microbiological ResearchVolume 192;Pages 130-14. https://doi.org/10.1016/j.micres.2016.06.007 from bee pollen: structure, absorption, metabolism.
Ghadimi‐Garjan, R., Javadi, A., Jafarizadeh‐Malmiri, H., Anarjan, N., & Mirzaei, H. (2023). Lyophilized royal jelly preparation in nanoscale and evaluation of its physicochemical properties and bactericidal activity. Food Science & Nutrition, 11(6), 3404–3413. https://doi.org/10.1002/fsn3.3330
Ghosh .S and Jung .CH.(2024).Chemical Composition and Nutritional Value of Royal Jelly Samples Obtained from Honey Bee (Apis mellifera) Hives Fed on Oak and Rapeseed Pollen Patties .MDPI; 15(3), 141. https://doi.org/10.3390/insects15030141
Guo, J., Wang, Z., Chen, Y., Cao, J., Tian, W., Ma, B., & Dong, Y. (2021). Active components and biological functions of royal jelly. Journal of Functional Foods, 82,
Helbing, S., Lattorff, H. M. G., Moritz, R. F., & Buttstedt, A. (2017). Comparative analyses of the major royal jelly protein gene cluster in three Apis species with long amplicon sequencing. DNA Research, 24(3), 279–287. https://doi.org/10.1093/dnares/dsw064
Hospodarova, V., Singovszka, E., & Stevulova, N. (2018). Characterization of cellulosic fibers by FTIR spectroscopy for their further implementation to building materials. American Journal of Analytical Chemistry, 09(06), 303–310. https://doi.org/10.4236/ajac.2018.96023
Ibrahim, H. R.; Nanbu, F. and Miyata, T. (2021). Potent antioxidant peptides derived from honey major protein enhance tolerance of eukaryotic cells toward oxidative stress. Food Production, Processing and Nutrition, 3 (11): 1-10.
Jaine .j., and Howse. S.(2019). WHAT IS DIASTASE ? Analytica Laboratories; RESEARCH. NEW ZEALAND BEEKEEPER, AUGUST 2019:14.
Jandrić, Z., Roberts, D., Rathor, M., Abrahim, A., Islam, M., and Cannavan, A. (2013). Assessment of fruit juice authenticity using UPLC–QToF MS: A metabolomics approach. Food Chemistry, 148, 7–17. https://doi.org/10.1016/j.foodchem.2013.10.014
Kanelis, D., Tananaki, C., Liolios, V., Dimou, M., Goras, G., Rodopoulou, M. A., Karazafiris, E., and Thrasyvoulou, A. (2015b). A suggestion for royal jelly specifications / Prijedlog globalnih standarda za matičnu mliječ. Archives of Industrial Hygiene and Toxicology, 66(4), 275–284. https://doi.org/10.1515/aiht-2015-66-2651.
Kanelis, D., Tananaki, C., Liolios, V., Rodopoulou, M., Goras, G., Argena, N., and Thrasyvoulou, A. (2018). Investigating the effect of supplementary feeding on carbohydrate composition and quantity of royal jelly. Open Journal of Applied Sciences, 08(04), 141–149. https://doi.org/10.4236/ojapps.2018.84011
Kasprzyk, I.; Depciuch, J.; Grabek-Lejko, D. and Parlinska-Wojtan, M. (2018). FTIR-ATR spectroscopy of pollen and honey as a tool for unifloral honey authentication. The case study of rape honey. Food Control., 84: 33–40.
Kausar S.H , More V.R .(2019). Royal Jelly: Organoleptic Characteristics and Physicochemical Properties. The Pharmaceutical and Chemical Journal:6(2):20-24.ISSN: 2349-7092.
Kazemi, V., Eskafi, M., Saeedi, M., Manayi, A., & Hadjiakhoondi, A. (2019). Physicochemical Properties of Royal Jelly and Comparison of Commercial with Raw Specimens. Jundishapur Journal of Natural Pharmaceutical Products, 14(4). https://doi.org/10.5812/jjnpp.64920
Kedare, S. B., and Singh R. P.( 2011). Genesis and development of DPPH method of antioxidant assay. J Food Sci Techol: 48 (4): 412 – 422.
Khalil , MD, I .; Sulaiman, S.A.; Alam, N.; Moniruzzaman ,M.; Bai’e ,S .; Man ,C.N .; Jamalullail ,S.M.S and Gan,S.H.(2012c). Gamma irradiation increases the antioxidant properties of tualang honey stored under different conditions. Molecules, 17: 674-687.
Kocot .J. , Kiełczykowska .M., Luchowska-Kocot.D., Kurzepa .J. and Irena Musik.(2018). Antioxidant Potential of Propolis, Bee Pollen, and Royal Jelly: Possible Medical Application .National Library of Medicine :2018 May 2;2018:7074209
Kolayli, S., Sahin, H., Can, Z., Yildiz, O., Malkoc, M., & Asadov, A. (2015). A member of Complementary Medicinal food. Journal of Evidence-Based Complementary & Alternative Medicine, 21(4), NP43–NP48. https://doi.org/10.1177/2156587215618832
Koike, H.; Kanda, M.; Hayashi, H.; Matsushima, Y.; Yoshikawa, S.; Ohba, Y. Hayashi, M.; Nagano, C.; Sekimura, K.; Otsuka, K.; Kamiie, J.; Sasamoto, T. and Hashimoto, t. (2020). Development of an alternative approach for detecting botulinum neurotoxin type A in honey: Analysis of non-toxic peptides with a reference labelled protein via liquid chromatographytandem mass spectrometry. Food Additives & Contaminants: Part A, 1-15.
Lee, C. H. (2017). A Simple outline of methods for protein isolation and purification. Endocrinol Metab., 32: 18-22.
Lee, S.; Norul , A.; Rahaman, N.A .; Adnan, S. and Titjih , E.T. (2013). Antioxidant activity of three honey samples in relation with their biochemical components hindawi publishing corporation. Journal of Analytical Methods in Chemistry, 313798.
Liu, J.R., Yang, Y.C., Shi, L.S. and Peng, C.C. (2008). Antioxidant Properties of Royal Jelly Associated with Larval Age and Time of Harvest. Alternnative Medicine Reviews, 13: 330‐3336.
Maghsoudlou, A., Mahoonak, A. S., Mohebodini, H., & Toldra, F. (2019). Royal Jelly : Chemistry, storage and bioactivities. Journal of Apicultural Science, 63(1), 17–40. https://doi.org/10.2478/jas-2019-0007
Mandacaru, S. C., Vale, L. H. F. D., Vahidi, S., Xiao, Y., Skinner, O. S., Ricart, C. a. O., Kelleher, N. L., De Sousa, M. V., and Konermann, L. (2017). Characterizing the structure and oligomerization of Major Royal Jelly protein 1 (MRJP1) by mass spectrometry and complementary biophysical tools. Biochemistry, 56(11), 1645–1655 . https: //doi.org /10.1021/ acs.biochem .7b00020
Martos, M.V., Navajas, Y.R., Lopez, J.F. and Perez-Alvarez, J.P. (2008). Functional Properties of Honey, Propolis, and Royal Jelly. Journal of Food Science, 73 (9): R117-24
Mesaik, M. A. ; Dastagir, N. ; Uddin, N. ; Rehman, K. and Azim, M. K. (2015). Characterization of immunomodulatory activities of honey glycoproteins and glycopeptides. Agric. Food Chem., 63, 177−184.
Mohiuddin, I., Kumar, T. R., Zargar, M. I., Wani, S. U. D., Mahdi, W. A., Alshehri, S., Alam, P., & Shakeel, F. (2022). GC-MS Analysis, Phytochemical Screening, and Antibacterial Activity of Cerana indica Propolis from Kashmir Region. Separations, 9(11), 363. https://doi.org/10.3390/separations9110363
Muli, E.; Munguti, A. and Raina, S. K. (2007). Quality of honey harvested and processed using traditional methods in rural areas of Kenya. Acta Vet. Brno., 76: 315–320.
Mureşan, C. I., and Buttstedt, A. (2019). pH-dependent stability of honey bee (Apis mellifera) major royal jelly proteins. Scientific Reports, 9(1). https://doi.org/10.1038/s41598-019-45460-0
Nabas, Z., Haddadin, M., Haddadin, J., & Nazer, I. (2014). Chemical Composition of Royal Jelly and Effects of Synbiotic with Two Different Locally Isolated Probiotic Strains on Antioxidant Activities. Polish Journal of Food and Nutrition Sciences, 64(3), 171–180. https://doi.org/10.2478/pjfns-2013-0015
Nabas, Z., Haddadin, M., Haddadin, J., & Nazer, I. (2014). Chemical Composition of Royal Jelly and Effects of Synbiotic with Two Different Locally Isolated Probiotic Strains on Antioxidant Activities. Polish Journal of Food and Nutrition Sciences, 64(3), 171–180. https://doi.org/10.2478/pjfns-2013-0015.
Nagmoti, D. M.; Khatri, D. K.; Juvekar, P. R. and Juvekar, A. R. (2012). Antioxidant activity free radical scavenging potential of Pithecellobium dulce Benth seed extracts. Free Radicals and Antioxidants, 2(2):37-43.
Nayik, G . and Nanda,V. (2015 ). Physico-chemical, enzymatic, mineral and colour characterization of three different varieties of honeys from Kashmir valley of india with a multivariate approach pol. J. Food Nutr. Sci., 65.(2): 101–108.
Negro, V., López-Gutiérrez, J., Esteban, M. D., & Matutano, C. (2013). Uncertainties in the design of support structures and foundations for offshore wind turbines. Renewable Energy, 63, 125–132. https://doi.org/10.1016/j.renene.2013.08.041
Oriolowo, O., John, O., Abubakar, D., Jonah, T., & Ismaila, D. (2020). Anti-nutritional Composition of Honey Samples from Four Northern States of Nigeria. Nigerian Journal of Basic and Applied Sciences, 27(2), 32–38. https://doi.org/10.4314/njbas.v27i2.5
Pal, G. K.and Suresh, P. (2016). Sustainable valorisation of seafood by-products: Recovery of collagen and development of collagen-based novel functional food ingredients. Innov. Food Sci. Emerg. Technol., 37, 201–215.
Pavel, C. I., Mărghitaş, L. A., Dezmirean, D. S., Tomoş, L. I., Bonta, V., Şapcaliu, A., & Buttstedt, A. (2014). Comparison between local and commercial royal jelly—use of antioxidant activity and 10-hydroxy-2-decenoic acid as quality parameter. Journal of Apicultural Research, 53(1), 116–123. https://doi.org/10.3896/ibra.1.53.1.12
Pérez, E.; Vit, P. and Huq, F. (2013). Flavonoids and polyphenols in studies of honey antioxidant activity. International Journal of Medicinal Plant and Alternative Medicine,1(4): 063-072. Prakonsepsi. Jurnal Keperawatan Muhammadiyah Edisi Khusus2020. Alamat Website: http://journal.um-surabaya.ac.id/index.php/JKM
Qu, N., Jiang, J., Sun, L., Lai, C., Sun, L., & Wu, X. (2008). Proteomic characterization of royal jelly proteins in Chinese (Apis cerana cerana) and European (Apis mellifera) honey bees. Biochemistry (Moscow), 73, 676.
Rahul .D , Lohidasan .S , Laxmi . R and Sandeep .S. (2023). Investigation of Nutraceutical Potential, in vitro Antioxidant and Free Radical Scavenging Activity of Indian Royal Jelly. Journal of Research in Pharmacy, 2023, Vol 27, Issue 3, p1289. ISSN: 2630-6344.
Ramadan .M and Al-Ghamdi .A. (2012). Bioactive compounds and health-promoting properties of royal jelly: A review. Journal of Functional Foods. Volume 4, Issue 1, Pages 39-52 https://doi.org/10.1016/j.jff.2011.12.007
Ramanathan .A., Nair. A. and Sugunan. V.(2018). A review on Royal Jelly proteins and peptides. Journal of Functional Foods: 44 (2018) 255–264. https://doi.org/10.1016/j.jff.2018.03.008
Rassu, G., Cossu, M., Langasco, R., Carta, A., Cavalli, R., Giunchedi, P., & Gavini, E. (2015). Propolis as lipid bioactive nano-carrier for topical nasal drug delivery. Colloids and Surfaces B: Biointerfaces, 136, 908–917. doi:10.1016/j.colsurfb. 2015.10.043.
Rzepecka-Stojko, A .,Stojko .J., Kurek-Górecka. A ., Górecki. M., Kabała-Dzik.A., Kubina.R., Moździerz. A. and Buszman.E .(2016).Polyphenols from Bee Pollen: Structure, Absorption, Metabolism and Biological Activity. Molecules 2015, 20, 21732-21749. DOI: 10.3390/molecules21020159.
Sabatini, A. G. (2009). Quality and standardisation of Royal Jelly. Journal of ApiProduct and ApiMedical Science, 1(1), 16.
Saeed, M. A. and Jayashankar, M. (2020). Physico-chemical characteristics of some Indian and Yemeni honey. Journal of Bioenergy and Food Science, 7(2), e2832019JBFS. doi: 10.18067/jbfs.v7i2.283.
Sánchez, A. and Vázquez, A. (2017). Bioactive peptides: A review. Food Quality and Safety, 1(1): 29–46.
Santos, K. S., dos Santos, L. D., Mendes, M. A., de Souza, B. M., Malaspina, O., & Palma, M. S. (2005). Profiling the proteome complement of the secretion from hypopharyngealgland of Africanized nurse-honey bees (Apis mellifera L.). Insect Biochemistry and Molecular Biology, 35, 85–91.
Serem, J.C. and Bester, M.J.(2012). Physicochemical properties, antioxidant activity and cellular protective effects of honeys from southern Africa. Food Chem., 133: 1544-1550.
Sesta, G.(2006). Determination of sugars in royal jelly by HPLC1. INRA/DIB-AGIB/ EDP Sciences, Apidologie 37 (2006) 84–90.
Sousa .M , Pereira .J , De Lima .L , Rezende .Th and Silva .A. (2025). Royal Jelly:A Brief Review of Nano and Micro Carriers and Potential Applications. International Journal of Environmental Chemistry :Volume 11, Issue 1. ISSN: 2456-5245.DOI (Journal): 10.37628/IJEC.
Srisuparbh, D.; Klinbunga, S.; Wongsiri, S. and Sittipraneed, S. (2003). Isolation and characterization of major royal jelly cdnas and proteins of the honey bee (Apis cerana). J. of Biochemistry and Molecular Biology, 36(6): 572-579.
Sugiyama .T , Takahashi .K. ,and Mori .H.(2012). Royal jelly acid, 10-hydroxy-trans-2-decenoic acid, as a modulator of the innate immune responses. National Library of Medicine: 12(4):368-76. doi:10.2174/187153012803832530.
Szczesna, T., Rybak-Chmielewska, H., Was, E., & Skubida, P. (2009). Water determination in bee products using the karl fischer titration method. Journal of ApiculturalScience, 53(2). http://yadda.icm.edu.pl/yadda/element/bwmeta1.element.dl-catalog-7c59d90b-c9af-46b9-8bad-f77d3d1c615c
Szweda, P. (2017). Antimicrobial Activity of Honey. In: the Book Honey Analysis, Chapter 5 http://dx.doi.org/10.5772/67117.
Taha, A. (2020). Profile analysis of major and minor honey contents from different african countries. Egypt. Acad. J. Biolog. Sci., 13(2): 269-281.
Takruri, H., and Alkhedr ,R.(2021). Determination of the total phenolic content, total antioxidant capacity and radical scavenging activity of Jordanian royal Jelly and honey samples. Jerash for Research and Studies 615. -022-001-021. https://doi.org/10.36091/0550
Tomczyk, M.; Bocian, A.; Sidor, E.; Miłek, M.; Zaguła, G. and Dzugan, M. (2022). The use of HPTLC and SDS-PAGE methods for coniferous honeydew honey fingerprinting compiled with mineral content and antioxidant activity. Molecules, 27, 720.
Tsao, R. (2010). Chemistry and biochemistry of dietary polyphenols .Nutrients, 2:1231-1246.
Umami .N., Raya .I., Usman .A., Azizah .and Eppang .Y.(2020). Hasil Uji Fitokimia: Kandungan Royal Jelly Apis Mellifera Sebagai Persiapan Suplemen
Uthurry, C. A., Hevia, D., & Gomez-Cordoves, C. (2011). Role of honey polyphenols in health. Journal of ApiProduct and ApiMedical Science, 3(4), 141–159. https://doi.org/10.3896/ibra.4.03.4.01
Valachova, I.; Buceková, M. and Majtán, J. (2016). Quantification of bee-derived peptide defensin-1 in honey by competitive enzyme-linked immunosorbent assay, a new approach in honey quality control. Czech J. Food Sci., 34.
Vulić, J., Čanadanović-Brunet, J., Ćetković, G., Djilas, S., & Šaponjac, V. T. (2015). Antioxidant and Sensorial Properties of Polyfloral Honey with Dried Apricots after One Year of Storage. Journal of Chemistry, 2015, 1–7 . https: /doi.org/10.1155/2015/858049
Weber, A. M.; Hans, W.and Pfleger, K. (2007). Mass spectral and GC data of drugs, poisons, pesticides, pollutants and their metabolites. Weinheim: Wiley-VCH.
Wytrychowski, M., Chenavas, S., Daniele, G., Casabianca, H., Batteau, M., Guibert, S., and Brion, B. (2013). Physicochemical characterisation of French royal jelly: Comparison with commercial royal jellies and royal jellies produced through artificial bee-feeding. Journal of Food Composition and Analysis, 29(2), 126–133. https://doi.org/10.1016/j.jfca.2012.12.002
Xue, X., Wu, L., and Wang, K. (2017b). Chemical composition of royal jelly. In Springer eBooks (pp. 181–190). https://doi.org/10.1007/978-3-319-59689-1_8.
Yelin .A. and Kuntadi.(2019). Phytochemical Identification of Honey from serveral regions in Java and Sumbawa.The Journal of Chemical Physics Reviews: Volume 2120, Issue1. AIP Conf. Proc. 2120, 080024 (2019). https://doi.org/10.1063/1.5115762 .
Yelin .A. and Kuntadi.(2019). Phytochemical Identification of Honey from serveral regions in Java and Sumbawa.The Journal of Chemical Physics Reviews: Volume 2120, Issue1. AIP Conf. Proc. 2120, 080024 (2019). https://doi.org/10.1063/1.5115762
Yen, G. C.; Duh, P. D. and Su, H. J. (2005). Antioxidant properties of lotus seed and its effect on DNA damage in human lymphocytes. Food Chem., 89: 379–385.
Yilamaz, H., and Kufrevioglu, I. (2001). Composition of honeys collected from eastern and south-eastern Anatolia and effect of storage on hydroxymethylfurfural content and diastase activity. Turk J. Agric., 25: 347-349.
Yu, X., Tu, X., Tao, L., Daddam, J., Li, S., and Hu, F. (2023). Royal Jelly Fatty acids: chemical composition, extraction, biological activity, and prospect. Journal of Functional Foods, 111, 105868. https://doi.org/10.1016/j.jff.2023.105868
Zhang L, Qi D, Ma Ch , Wang W, ,Hao J, Li J,(2020). Gas chromatography-mass spectrometry analysis reveals the differences in volatile components of royal jelly from different honeybee stocks. LWT, Volume 124, 109143.
Zhang, L., Fang, Y., Li, R., Feng, M., Han, B., Zhou, T., and Li, J. (2012). Towards posttranslational modification proteome of royal jelly. Journal of Proteomics, 75(17), 5327–5341. https://doi.org/10.1016/j.jprot.2012.06.008
Zhu, Z., Zhang, Y., Wang, J., Li, X., Wang, W., & Huang, Z. (2019b). Characterization of sugar composition in Chinese royal jelly by ion chromatography with pulsed amperometric detection. Journal of Food Composition and Analysis, 78, 101–107. https://doi.org/10.1016/j.jfca.2019.01.003

